题目内容
铜镁合金具有优良的导电性,常用作飞机天线等导电材料。欲测定合金的组成(其他元素忽略不计),进行如下实验,取铜合金2 0 g放入烧杯,将280 g稀硫酸分4次加入烧杯,充分反应后,测得剩余固体的质量记录如下。请计算:
0 g放入烧杯,将280 g稀硫酸分4次加入烧杯,充分反应后,测得剩余固体的质量记录如下。请计算:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
| 剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(1)合金中铜、镁的质量比为________。
(2)所加稀硫酸的溶质质量分数。(写出计算过程)
(1)33∶17 (2)解:分析表中数据知:与70 g稀硫酸完全反应消耗镁的质量为1.8 g。
设与1.8g镁反应的稀硫酸的溶质质量为x。
Mg+H2SO4 MgSO4+H2↑
MgSO4+H2↑
24 98
1.8 g x
 =
= x=7.35 g
x=7.35 g
稀硫酸的溶质质量分数为: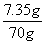 ×100%=1
×100%=1 0.5%
0.5%
答 :所加稀硫酸的溶质质量分数为10.5%。
:所加稀硫酸的溶质质量分数为10.5%。

某氢氧化钙中含碳酸钙杂质。称取研细的该样品12.4 g放入锥形瓶中,加入32.6 g的水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生。测得加入盐酸的质量与锥形瓶中的物质的质量关系如下表所示。
| 加入盐酸的质量/g | 0 | 25 | 37.5 |
| 锥形瓶中物质的质量/g | 45 | 70 | 80.3 |
(1)加入盐酸的质量在0~25 g时,_______与盐酸发生反应。
(2)反应产生二氧化碳的质量为________g。
(3)求样品中氢氧化钙的质量分数。(写出计算过程,精确到0.1%)
KNO3与K Cl的溶解度曲线如右图所示,请回答下列问题:
Cl的溶解度曲线如右图所示,请回答下列问题:
 ①t2℃时,KNO3的溶解度 (9) KCl的溶解度
①t2℃时,KNO3的溶解度 (9) KCl的溶解度
(填“>”、“<”或“=”)。
②t1℃时,将50g KNO3加入 (10) g水中,完全溶解后,
恰好得到饱和溶液。要进一步提高该溶液的溶质质量分数,
可进行的操作是 (11) 。
③KNO3溶液中含有少量KCl时,可通过 (12 ) 的方法提纯。
) 的方法提纯。
④实验室可 用化学方法来鉴别KNO3与KC溶液,请用化学方程式表示其原理 (13) 。
用化学方法来鉴别KNO3与KC溶液,请用化学方程式表示其原理 (13) 。
⑤在一定温度下,向100克水中依次加入一定质量的KCl固体,充分溶解,所加KCl的质量与得到相应溶液的质量关系如下图所示:
 |
Ⅰ.实验②的溶液是否为饱和溶液? (14) (填“是”、“不是”或“无法判断”)。
Ⅱ.实验①、②、③所得溶液的溶质质量分数分别表示为a%、b%、c%,则a、b、c的大小关系是 (15) (用“>”、“<”或“=”表示)。
