题目内容
2.某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.探究一:甲同学设计了如下实验方案,请你帮助完成实验报告.
| 方案 | (1) | (2) | (3) |
| 实验操作 |  | 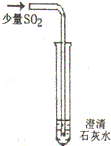 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水、二氧化硫与澄清石灰水反应的化学方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氢氧化钙溶液能与酸发生中和反应 |
【查阅资料】CaCl2溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含有少量酚酞外,溶质可能有以下三种情况:①CaCl2②CaCl2和HCl③CaCl2和Ca(OH)2.
【分析讨论】丙同学从实验现象分析得出:猜想③肯定不合理,其理由是稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙.
探究二:
丁同学进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴边振荡,实验后得出产生沉淀质量与滴加碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀.
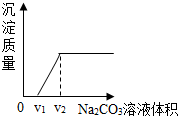
【得出结论】乙同学的猜想中,②(填序号)合理.
【反思讨论】
学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化,下列说法正确的是AB(填序号).
A.溶液质量逐渐增大 B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小 D.溶液的pH一直在增大.
分析 探究一:
(1)根据碱性溶液能使紫色石蕊溶液变蓝解答;
(2)根据氢氧化钙溶液能与某些非金属氧化物反应生成盐和水解答;
【分析讨论】根据稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性解答;
探究二:根据图示现象分析解答.
【得出结论】根据实验探究得出结论;
【反思讨论】根据碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳解答;根据碳酸钠和氯化钙反应,生成碳酸钙沉淀、氯化钠解答.
解答 解:探究一:
(1)澄清的石灰水显碱性,碱性溶液能使紫色石蕊溶液变蓝;
(2)二氧化硫和氢氧化钙反应,生成亚硫酸钙和水,反应的化学方程式是SO2+Ca(OH)2═CaSO3↓+H2O;
【分析讨论】从实验现象分析可知:稀盐酸加入滴有酚酞的石灰水中,红色褪为无色,说明溶液为中性或酸性,不可能有氢氧化钙,故猜想③肯定不合理;
探究二:根据图示现象分析可知:因稀盐酸过量,故加入碳酸钠后首先与过量的稀盐酸反应,产生气泡,然后再与氯化钙反应,生成的碳酸钙沉淀,溶液最终变红色;
【得出结论】根据实验探究可知:溶液中除含少量酚酞外,溶质有CaCl2和HCl,故②正确;
【反思讨论】碳酸钠和稀盐酸反应,生成氯化钠、水和二氧化碳;碳酸钠和氯化钙反应,生成碳酸钙沉淀、氯化钠,故:
A、不断滴加碳酸钠溶液,溶液质量逐渐增大,故对;
B、氯化钠质量逐渐增大,V2后反应完全,保持不变,故对;
C、氯化钙的质量逐渐减小,故错;
D、溶液的pH一直在增大,最后不变,故错.
答案:
| 方案 | (1) | (2) | (3) |
| 实验操作 |  |  |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氢氧化钙溶液能与酸发生中和反应 |
探究二:滴加碳酸钠溶液,开始先产生气泡,随后才产生沉淀.
【得出结论】②;
【反思讨论】AB.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.

练习册系列答案
相关题目
10.实验是学习化学的一条重要途径.下列化学实验操作正确的是( )
| A. | 用滴管向试管内加入少量液体 | |
| B. | 用手捂住试管检验装置气密性 | |
| C. | 将燃着的木条伸入集气瓶中检验二氧化碳是否收集满 | |
| D. | 将浓硫酸沿着烧杯内壁慢慢倒入水中,并用玻璃棒搅拌 |
17.化学知识在生活中有着广泛的应用,下列说法不正确的是( )
| A. | 血红蛋白质中含有铁元素,缺铁会引起人体贫血 | |
| B. | 回收废弃的塑料可以减少白色污染 | |
| C. | NaCl和NaNO2有咸味,都可用作食物的调味品 | |
| D. | 在发酵的面团中加入小苏打以提高馒头的口感和除去酸味 |
7.下列选项中,物质的名称、俗名、化学式不完全一致的是( )
| A. | 碳酸钠-纯碱-Na2CO3 | B. | 亚硝酸钠-食盐-NaNO2 | ||
| C. | 氢氧化钙-消石灰-Ca(OH)2 | D. | 氢氧化钠-烧碱-NaOH |
12.稀硫酸和氢氧化钠反应没有明显现象,老师在课堂上欲带领同学们设计实验证明它们之间发生了化学反应.
(1)请写出氢氧化钠与稀硫酸反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
(2)李海提出可以通过测量在稀硫酸溶液中不断滴加氢氧化钠溶液过程中溶液pH的变化得出结论,请描述测量溶液pH的方法用玻璃棒沾取待测溶液,涂在pH试纸上,观察变色情况,并于比色卡对照确定pH.
(3)化学反应过程中通常伴随有能量变化,查阅资料发现中和反应是放热反应.刘梅同学提出可以利用在氢氧化钠固体中滴加稀硫酸,测量反应过程中温度的变化情况达到实验的目的.这一方案立即被同学们认为不完善.你认为方案不完善的原因是氢氧化钠固体溶解放热,
给实验带来干扰.大家一起讨论了实验改进方案,大家都认为该实验要得到科学的结论需要控制相等的量是反应前酸、碱溶液温度相同.随后大家根据科学的方案重新进行了实验.实验中温度随滴加稀硫酸溶液体积变化情况记录如下表:
分析以上数据,氢氧化钠完全反应时消耗的稀硫酸溶液的体积是6ml;一段时间后,温度降低的原因是硫酸过量,由于热传递,导致温度降低.
(4)请设计出两种不同的实验方法证明氢氧化钠溶液中加入稀硫酸两者发生反生了化学反应.
方法一:氢氧化钠溶液中滴入几滴酚酞试液,再逐滴加入稀硫酸,溶液由红色变为无色,说明二者发生了化学反应.
方法二:在氢氧化钠溶液中加入过量的稀硫酸,然后加入硫酸铜,没有蓝色沉淀生成,说明两者发生了化学反应.
(1)请写出氢氧化钠与稀硫酸反应的化学方程式2NaOH+H2SO4=Na2SO4+2H2O.
(2)李海提出可以通过测量在稀硫酸溶液中不断滴加氢氧化钠溶液过程中溶液pH的变化得出结论,请描述测量溶液pH的方法用玻璃棒沾取待测溶液,涂在pH试纸上,观察变色情况,并于比色卡对照确定pH.
(3)化学反应过程中通常伴随有能量变化,查阅资料发现中和反应是放热反应.刘梅同学提出可以利用在氢氧化钠固体中滴加稀硫酸,测量反应过程中温度的变化情况达到实验的目的.这一方案立即被同学们认为不完善.你认为方案不完善的原因是氢氧化钠固体溶解放热,
给实验带来干扰.大家一起讨论了实验改进方案,大家都认为该实验要得到科学的结论需要控制相等的量是反应前酸、碱溶液温度相同.随后大家根据科学的方案重新进行了实验.实验中温度随滴加稀硫酸溶液体积变化情况记录如下表:
| 稀硫酸溶液体积(ml) | 0 | 2 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 温度(℃) | 20 | 20.5 | 24 | 24.8 | 25.2 | 24.3 | 23.6 | 21 | 20 |
(4)请设计出两种不同的实验方法证明氢氧化钠溶液中加入稀硫酸两者发生反生了化学反应.
方法一:氢氧化钠溶液中滴入几滴酚酞试液,再逐滴加入稀硫酸,溶液由红色变为无色,说明二者发生了化学反应.
方法二:在氢氧化钠溶液中加入过量的稀硫酸,然后加入硫酸铜,没有蓝色沉淀生成,说明两者发生了化学反应.