题目内容
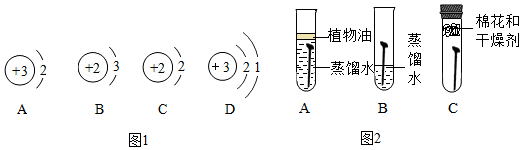
4.取一定量的饱和氯化钠溶液A放于烧杯中.加入一小粒高锰酸钾晶体.溶解后得到紫红色溶液B.再加入一小粒高锰酸钾晶体.继续溶解后得到紫红色溶液C.则溶液B是氯化钠的饱和溶液.却是高锰酸钾的不饱和溶液(填.“饱和”或“”不饱”).由此.你对饱和溶液的认识是在一定条件下,某物质的饱和溶液不能再溶解该物质,但可能再溶解其他物质.分析 根据饱和溶液和不饱和溶液的定义来分析判断,并作出正确的解答.
解答 解:取一定量的饱和氯化钠溶液A放于烧杯中,加入一小粒高锰酸钾晶体,溶解后得到紫红色溶液B.再加入一小粒高锰酸钾晶体,继续溶解后得到紫红色溶液C.则溶液B是氯化钠的饱和溶液,却为高锰酸钾的不饱和溶液,从而我们可以知道在一定条件下,某物质的饱和溶液不能再溶解该物质,但可能再溶解其他物质.
故答案为:饱和;不饱和;在一定条件下,某物质的饱和溶液不能再溶解该物质,但可能再溶解其他物质.
点评 熟练掌握饱和溶液和不饱和溶液的定义,并能够分析判断溶液是否饱和,难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
14.三聚氰胺是一种化工原料,含氮量高.今年我国发生婴幼儿奶粉污染事件就是造假者在奶粉中添加三聚氰胺以提高奶粉中含氮量,造成奶粉中蛋白质含量较高的假象,导致一些婴幼儿肾结石的食品安全事故.下列对于三聚氰胺(化学式为C3H6N6)认识中正确的是( )
| A. | 三聚氰胺由碳、氢、氮三种元素组成 | |
| B. | 每个三聚氰胺分子中含有3个氢分子 | |
| C. | 三聚氰胺中碳、氢、氮元素的质量比为1:3:3 | |
| D. | 三聚氰胺中氮元素的质量分数为33.3% |
15.下列说法完全正确的是( )
①为了增加肥效,将铵态氮肥和熟石灰共用
②日常生活中蒸馒头用的纯碱不是碱而是盐
③房屋失火,用水扑灭是因为降低了可燃物的着火点
④CO、SO2、氮的氧化物和CO2都是空气污染物
⑤氧气能与大多数物质发生反应即氧气的化学性质比较活泼
⑥合金的熔点和硬度通常比组成合金的纯金属熔点低,硬度大
⑦加碘食盐中添加的碘是单质.
①为了增加肥效,将铵态氮肥和熟石灰共用
②日常生活中蒸馒头用的纯碱不是碱而是盐
③房屋失火,用水扑灭是因为降低了可燃物的着火点
④CO、SO2、氮的氧化物和CO2都是空气污染物
⑤氧气能与大多数物质发生反应即氧气的化学性质比较活泼
⑥合金的熔点和硬度通常比组成合金的纯金属熔点低,硬度大
⑦加碘食盐中添加的碘是单质.
| A. | ①②④⑤ | B. | ②⑥⑦ | C. | ②③⑤ | D. | ②⑤⑥ |
12.生活离不开化学,下列选项中合理的是( )
| A. | 食用甲醛浸泡过的海产品,可提高人体免疫力 | |
| B. | 服用含有氢氧化铝的药物,治疗胃酸过多症 | |
| C. | 为了节约粮食,把霉变大米淘洗后食用 | |
| D. | 青少年适量补铁,可以预防佝偻病 |
9. 根据如图,天平游码的正确读数为( )
根据如图,天平游码的正确读数为( )
 根据如图,天平游码的正确读数为( )
根据如图,天平游码的正确读数为( )| A. | 1 g | B. | 2.8 g | C. | 2.6 g | D. | 3.0 g |
16.下列分析判断正确的是( )
| A. | 酸能够使紫色石蕊溶液变红,二氧化碳能使紫色石蕊溶液变红色,所以二氧化碳是酸 | |
| B. | 铁、铜都是金属单质,都能够置换出盐酸、稀硫酸中的氢 | |
| C. | 氧化物中含有氧元素,但是含有氧元素的化合物不一定是氧化物 | |
| D. | 硝酸铵和氢氧化钙混合使用能提高氮肥的肥效 |
13.下列说法错误的是( )
| A. | 在人类食物所供给的总能量中,有60%-70%来自于油脂 | |
| B. | 白糖、冰糖、红糖的主要成分就是蔗糖 | |
| C. | 很多食品发生霉变后,滋生的黄曲霉菌有很强的毒性 | |
| D. | 糖类是人类食物的主要成分,是由C、H、O三种元素组成的化合物 |
6.某化学兴趣小组同学在回收废旧电池的同时,开展了如下的实验探究.
【查阅资料】废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.
【实验1】废干电池的拆卸与处理
(1)兴趣小组同学将废旧干电池卸下的锌筒、碳棒冲洗干净,备用.
(2)将铜帽放入盐酸中,除去锈污,冲洗备用.
【实验2】检验废干电池筒内黑色固体中MnO2的存在
兴趣小组同学设计了如图所示的实验:
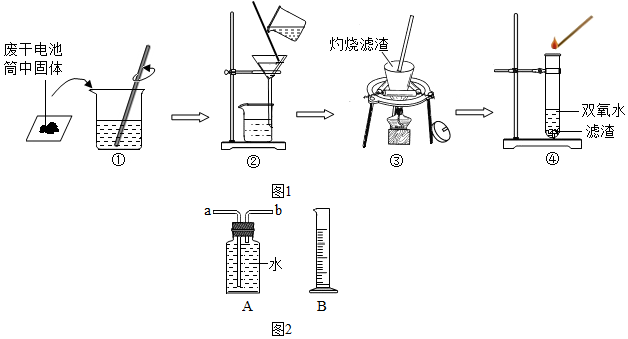
(1)操作②中过玻璃棒的作用是引流.
(2)引流操作③灼烧黑色滤渣时,会产生一种气体能使澄清石灰水变浑浊,该反应的化学表达式为CO2.
(3)操作④试管中产生的气体能使带火星木条复燃,该气体为O2
(4)由此得出结论:滤渣中黑色固体化学式为MnO2和C
【实验3】利用回收锌皮制取氢气及相关探究
(1)用锌皮和稀硫酸制取氢气.用适当的发生装置,采用排水法收集并测定氢气的体积(如图2),气体从装置A导管口b(填“a”或“b”) 进,选用仪器B测量排出水的体积,仪器B名称是量筒.
(2)探究影响锌与稀硫酸反应快慢的因素.反应过程中用前10min 内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表4组实验,获得数据如下.
[数据分析]
①比较实验a和实验b得到的结论是:与同体积同浓度的稀硫酸反应,含杂质的锌比纯锌反应速率大.
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和c(填实验编号).
③探究影响该反应快慢的因素,还需控制的条件是:温度(或锌粒形状大小)(举一例即可).
【实验4】探究经处理干净的二氧化锰在氯酸钾分解反应中的催化作用
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热.
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体.
(3)再将残留固体经溶解、过滤、洗涤、干燥、称量,得到5.5g黑色固体.
[数据分析]
①该实验说明:二氧化锰在氯酸钾分解反应前后,质量不变.
②完全反应后制得氧气的质量是9.6g.(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后生成各生成物的质量总和)
[实验反思]
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较产生氧气速率的大小.
【查阅资料】废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.
【实验1】废干电池的拆卸与处理
(1)兴趣小组同学将废旧干电池卸下的锌筒、碳棒冲洗干净,备用.
(2)将铜帽放入盐酸中,除去锈污,冲洗备用.
【实验2】检验废干电池筒内黑色固体中MnO2的存在
兴趣小组同学设计了如图所示的实验:

(1)操作②中过玻璃棒的作用是引流.
(2)引流操作③灼烧黑色滤渣时,会产生一种气体能使澄清石灰水变浑浊,该反应的化学表达式为CO2.
(3)操作④试管中产生的气体能使带火星木条复燃,该气体为O2
(4)由此得出结论:滤渣中黑色固体化学式为MnO2和C
【实验3】利用回收锌皮制取氢气及相关探究
(1)用锌皮和稀硫酸制取氢气.用适当的发生装置,采用排水法收集并测定氢气的体积(如图2),气体从装置A导管口b(填“a”或“b”) 进,选用仪器B测量排出水的体积,仪器B名称是量筒.
(2)探究影响锌与稀硫酸反应快慢的因素.反应过程中用前10min 内收集的氢气体积比较反应的快慢.控制其他条件相同,进行下表4组实验,获得数据如下.
| 实验编号 | 试剂 | 前10 min内产生的 氢气体积(mL) | |
| 锌的纯度 | 稀硫酸的体积和浓度 | ||
| a | 纯锌 | 30 mL 30% | 564.3 |
| b | 含杂质的锌 | 30 mL 30% | 634.7 |
| c | 纯锌 | 30 mL 20% | 449.3 |
| d | 纯锌 | 40 mL 30% | 602.8 |
①比较实验a和实验b得到的结论是:与同体积同浓度的稀硫酸反应,含杂质的锌比纯锌反应速率大.
②为了研究硫酸浓度对反应快慢的影响,需比较实验a和c(填实验编号).
③探究影响该反应快慢的因素,还需控制的条件是:温度(或锌粒形状大小)(举一例即可).
【实验4】探究经处理干净的二氧化锰在氯酸钾分解反应中的催化作用
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热.
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体.
(3)再将残留固体经溶解、过滤、洗涤、干燥、称量,得到5.5g黑色固体.
[数据分析]
①该实验说明:二氧化锰在氯酸钾分解反应前后,质量不变.
②完全反应后制得氧气的质量是9.6g.(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后生成各生成物的质量总和)
[实验反思]
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较产生氧气速率的大小.