题目内容
15.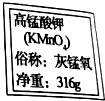 某同学准备用高锰酸钾制取氧气,他取出没开封的高锰酸钾试剂.看到瓶上标签如图所示.
某同学准备用高锰酸钾制取氧气,他取出没开封的高锰酸钾试剂.看到瓶上标签如图所示.(1)请计算该瓶高锰酸钾含氧元素多少克?
(2)若制取4g氧气,需要高锰酸钾多少克?
分析 (1)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答;
(2)由氧气的质量根据高锰酸钾分解的化学方程式可以计算出高锰酸钾的质量.
解答 解:
(1)316g高猛酸钾中含氧元素的质量为316g×$\frac{16×4}{316}×$100%=64g;
(2)设需要高锰酸钾的质量为x.
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 4g
$\frac{316}{x}=\frac{32}{4g}$
x=39.5g
答案:
(1)该瓶高锰酸钾含氧元素64g;
(2)若制取4g氧气,需要高锰酸钾39.5g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
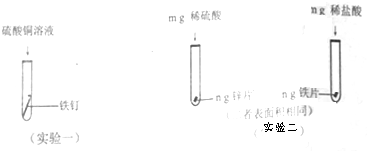
6.下列四个化学反应中,有一个反应的类型与其它三个不同.这个反应是( )
| A. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | B. | CuO+CO═Cu+CO2 | ||
| C. | H2SO4+Zn=Zn SO4+H2↑ | D. | CuCl2+Fe═FeCl2+Cu |
3.用化学方程式解释生活或生产中的现象,下列化学方程式书写正确的是( )
| A. | 用熟石灰抹的墙时间长了会变硬 CaO+H2O═Ca(OH)2 | |
| B. | 把含盐酸的洁厕灵滴到大理石地面有气泡 CaCO3+HCl═CaCl2+H2O+CO2↑ | |
| C. | 实验室用氯酸钾制氧气 2KClO3═2 KCl+3O2↑ | |
| D. | 成语“千锤百炼”是把铁炼成钢的过程C+O2 $\frac{\underline{\;点燃\;}}{\;}$ CO2 |
 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求: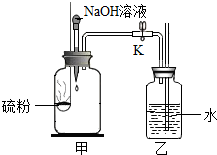 实验小组用图所示装置进行实验.实验步骤如下:
实验小组用图所示装置进行实验.实验步骤如下: 如图所示是电解水的实验装置图,请回答:
如图所示是电解水的实验装置图,请回答: