题目内容
6.根据如图回答问题.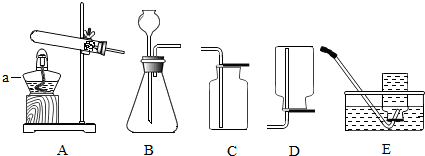
(1)实验仪器a的名称是酒精灯.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
所选用的发生装置是A.
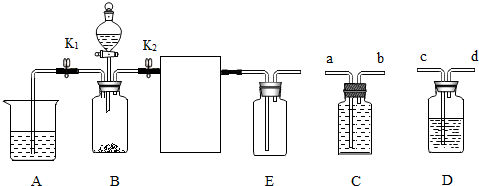
(3)实验室制取并收集二氧化碳选用的装置是BC,检验二氧化碳是否收集满的方法是将燃着的木条放在集气瓶口,木条熄灭,证明已收满.
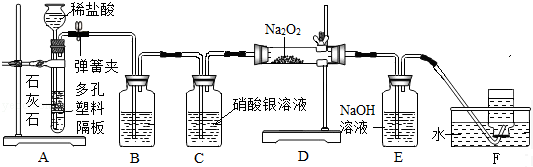
(4)某小组同学利用下图所示装置探究铁丝生锈的条件,其中C、D的分液漏斗中为足量且浓度和体积均相同的稀盐酸.
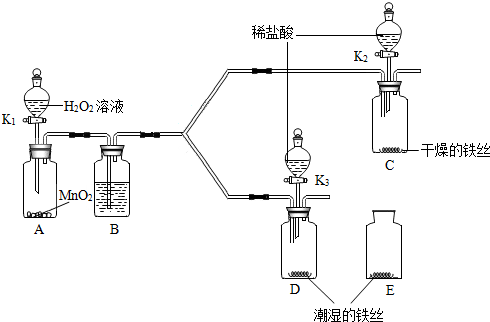
①步骤一:关闭K2和K3,打开K1,A中产生大量气泡. 为保证后续实验的成功,B中所盛放的溶液是浓硫酸.对比铁丝表面的变化,能够说明铁丝生锈与水有关的最佳装置是CD(填“C”、“D”或“E”,下同),能够说明铁丝生锈的快慢与氧气浓度有关的装置是DE.
②步骤二:关闭K1,打开K2和K3,将装置C、D中分液漏斗内的稀盐酸同时全部注入广口瓶中,C瓶中现象是固体溶解,有气泡产生,溶液由无色变成浅绿色;D瓶中溶液变成黄色反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,由此也可以判断铁丝生锈情况.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石和石灰石的主要成分是碳酸钙,通常情况下,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳; 二氧化碳能够溶于水,密度比空气大,不能燃烧,不支持燃烧.
(4)根据探究铁生锈的条件结合化学方程式的书写分析;根据题中提供的信息分析研究铁生锈的条件;
钢铁生锈的条件是钢铁与氧气和水同时接触.根据反应物和生成物及其质量守恒定律可以书写化学方程式.
解答 解:(1)实验仪器a的名称是酒精灯,常用作热源.
故填:酒精灯.
(2)实验室用高锰酸钾制取氧气的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
利用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置.
故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A.
(3)碳酸钙和稀盐酸反应不需要加热,应该用B装置作为发生装置;
二氧化碳能溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用C装置收集;
检验二氧化碳是否收集满的方法是:把燃烧的木条放在集气瓶口,如果燃烧的木条熄灭,说明已经收集满.
(4)①因为收集氧气时,可以用浓硫酸干燥.对比铁丝表面的变化,能够说明铁生锈与水可以用干燥和潮湿两种铁丝;铁生锈的快慢与氧气浓度有关的是纯净氧气和空气中的氧气;
②铁单独与氧气接触或与水接触时不容易生锈,与水和氧气同时接触时容易生锈.故C中铁不生锈,其化学方程式是Fe+2HCl=FeCl2+H2↑;D中铁生锈,生成氧化铁,与盐酸反应生成氯化铁;反应的化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. 浓硫;C D; D E;
(2)Fe+2HCl=FeCl2+H2↑;FeCl3
答案:
(1)酒精灯;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ A
(3)BC; 将燃着的木条放在集气瓶口,木条熄灭,证明已收满;
(4)①浓硫酸; CD; DE;
②固体溶解,有气泡产生,溶液由无色变成浅绿色,Fe2O3+6HCl=2FeCl3+3H2O
点评 本题考查仪器的用途、装置的选择、化学方程式的书写、实验基本操作等方面的知识,只有综合掌握教材内容才能正确的做出解答.

| A. | 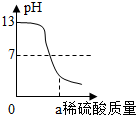 将锌片插入盛有一定量稀硫酸的烧杯中 将锌片插入盛有一定量稀硫酸的烧杯中 | |
| B. | 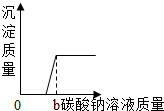 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| C. | 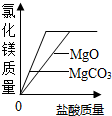 向足量碳酸镁和氧化镁固体中分别加入相同质量、相同质量分数稀盐酸中 向足量碳酸镁和氧化镁固体中分别加入相同质量、相同质量分数稀盐酸中 | |
| D. | 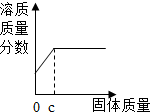 向盛有一定量稀盐酸的烧杯中不断滴入NaOH溶液至过量 向盛有一定量稀盐酸的烧杯中不断滴入NaOH溶液至过量 |
| A. | 氦气:He | B. | 氧化铁:FeO | C. | 氢氧化钾:KOH | D. | 碳酸:H2CO3 |
| A. | 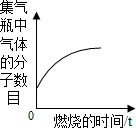 少量的硫磺在密闭的集气瓶中与氧气完全燃烧 | |
| B. | 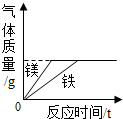 常温下,少量等质量的镁、铁分别同时放入足量等质量、等质量分数的稀盐酸中 | |
| C. | 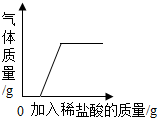 向部分变质的NaOH溶液中滴加过量稀盐酸 | |
| D. | 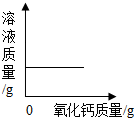 一定温度时,向一定量饱和石灰水中加入氧化钙 |
| A. | 不能用金属铜与稀硫酸反应制取氢气 | |
| B. | 银的导电性强于铜 | |
| C. | 铜能将银从硝酸银溶液中置换出来 | |
| D. | 在空气中铁比铜易生锈 |