题目内容
15.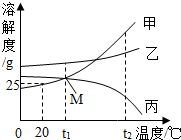 如图为甲、乙、丙三种固体物质的溶解度曲线.试根据图中所给信息回答下列问题:
如图为甲、乙、丙三种固体物质的溶解度曲线.试根据图中所给信息回答下列问题:(1)点M表示t1℃时甲丙的溶解度相等;
(2)温度为t2℃时,甲、乙、丙三种物质溶解度由大到小的顺序为甲>乙>丙;
(3)20℃时,在50g水中加入25g物质甲,得到甲溶液的质量为62.5g;
(4)20℃时,将甲、乙、丙三种物质的饱和溶液升高到t2℃时,所得溶液的溶质质量分数由小到大的顺序为丙<甲<乙.
(5)若甲中含有少量乙,应用降温结晶(或冷却热饱和溶液)法提纯.
分析 (1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(3)据该温度下甲的溶解度分析解答;
(4)据饱和溶液中溶质的质量分数分析解答,并结合三种物质的溶解度随温度的变化情况分析升温后溶质的质量分数大小关系;
(5)据甲乙的溶解度受温度影响情况分析解答.
解答 解:(1)M点是甲丙在t1℃时溶解度曲线的交点,表示t1℃时甲丙的溶解度相等;
(2)温度为t2℃时,甲、乙、丙三种物质溶解度由大到小的顺序为 甲>乙>丙;
(3)20℃时甲的溶解度是25g,即100g水中最多溶解25g的甲,所以在50g水中加入25g物质甲,最多溶解12.5g,得到甲溶液的质量为62.5g;
(4)20℃时,将甲、乙、丙三种物质的饱和溶液升高到t2℃时,甲乙的溶解度变大,溶液中溶质、溶剂的质量不变,溶质的质量分数不变,丙的溶解度变小,析出晶体,溶质的质量分数减小;饱和溶液中溶质 的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,可知溶解度大则溶质的质量分数大,而20℃时乙的溶解度大于甲的溶解度大于t2℃时丙的溶解度,故所得溶液的溶质质量分数由小到大的顺序为丙<甲<乙;
(5)甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,所以若甲中含有少量乙,应用冷却热饱和溶液或降温结晶的方法提纯甲;
故答案为:(1)t1℃时甲丙的溶解度相等;
(2)甲>乙>丙;
(3)62.5g;
(4)丙<甲<乙;
(5)降温结晶(或冷却热饱和溶液).
点评 掌握溶解度、溶解度曲线的意义并会应用分析解决相关问题,考查了学生应用知识解答问题的能力,饱和溶液中溶解度越大质量分数也就越大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.在一密闭容器中放入甲、乙、丙、丁四种物质,一定条件下使其发生化学反应,通过传感设备测得反应一段时间后的部分数据如表,下列说法不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | X | 26 | 2 | 12 |
| A. | 乙是反应物 | B. | 反应后物质甲的质量为13g | ||
| C. | 参加反应的甲和丁的质量比为1:4 | D. | 物质丙可能是该反应的催化剂 |
3.下列对“化学与生活”的认识,不正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
20.空气中氮气的体积分数大约是( )
| A. | 78% | B. | 21% | C. | 0.94% | D. | 0.03% |
5.下列变化中不是由小分子转化为高分子的是( )
| A. | 葡萄糖转化为淀粉 | |
| B. | 乙烯转化为聚乙烯 | |
| C. | 铜、氧气、水和二氧化碳转化为碱式碳酸铜[Cu2(OH)2CO3] | |
| D. | 氨基酸转化为蛋白质 |