题目内容
12. 下列字母 A--H 表示初中化学常见的物质,它们由氢、碳、氧、氯、钠、钙、铁中的 2-3 种元素组成.
下列字母 A--H 表示初中化学常见的物质,它们由氢、碳、氧、氯、钠、钙、铁中的 2-3 种元素组成.(1)A有强烈的腐蚀性,易潮解,无色酚酞溶液遇A的 稀溶液变红,A的俗称是烧碱.
(2)红色粉末B与气体C反应得到黑色粉末,化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
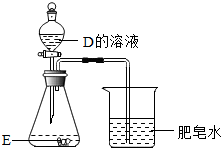
(3)D和E均含两种元素.如图所示,将D的溶液滴入锥形瓶中,溶液变黄,有气泡产生;烧杯中聚集的肥皂泡能被点燃.E中含有的元素是Fe、O,锥形瓶中发生反应的化学方程式为Fe+2HCl=FeCl2+H2↑,Fe2O3+6HCl=2FeCl3+3H2O.
分析 (1)根据A的性质有强烈的腐蚀性,易潮解,无色酚酞溶液遇A的稀溶液变红,可推断出A是氢氧化钠,俗称烧碱、火碱、苛性钠进行分析;
(2)根据红色粉末是氧化铁,能与氢气、一氧化碳、碳等反应进行分析;
(3)根据溶液变黄可知反应物中含有铁元素,有气泡产生且可燃得出生成了氢气,说明反应物中含有氢元素进行分析.
解答 解:(1)根据A的性质有强烈的腐蚀性,易潮解,无色酚酞溶液遇A的稀溶液变红,可推断出A是氢氧化钠,俗称是烧碱;
(2)红色粉末是氧化铁,能与一氧化碳反应反应生成单质的铁和二氧化碳,注意C不能是氢气,因为题目要求是2-3种元素组成,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)由溶液变黄可知反应物中含有铁元素且发生的是复分解反应;有气泡产生且可燃,判断生成了氢气且发生的是置换反应,说明反应物中含有氢元素,可推断是生锈的铁与D稀盐酸反应,铁和盐酸反应生成氯化亚铁和氢气,氧化铁和盐酸反应生成氯化铁和水,化学方程式为:Fe+2HCl═FeCl2+H2↑,Fe2O3+6HCl═2FeCl3+3H2O.
故答案为:(1)烧碱;
(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)Fe、O,Fe+2HCl=FeCl2+H2↑,Fe2O3+6HCl=2FeCl3+3H2O.
点评 本题的推断由组成物质的元素做为限定条件,因此,熟悉常见物质的组成、性质及变化规律对该题中所涉及物质的推断就至关重要了.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
2.下列事实能用物理变化解释的是( )
| A. | 水壶烧水出现水垢 | |
| B. | 烧碱变质 | |
| C. | 活性炭除冰箱中的异味 | |
| D. | 用石灰浆粉刷墙壁,干燥后墙面变硬 |
20.下列事实用微粒的知识解释正确的是( )
| 选项 | 事 实 | 解 释 |
| A | 空气是混合物 | 由不同种原子构成 |
| B | CO和 CO2的化学性质不同 | 构成分子的原子的种类不同 |
| C | 等质量的水蒸气与冰的体积不同 | 构成物质的水分子间的间隔不同 |
| D | 石油分馏得到不同的产品 | 分子的种类发生改变 |
| A. | A | B. | B | C. | C | D. | D |
4.在一定条件下,下列物质不能和氧化铜反应的是( )
| A. | 碳单质 | B. | 一氧化碳 | C. | 稀硝酸 | D. | 氢氧化钠溶液 |
1.下列图象关系合理的是( )
| A. | 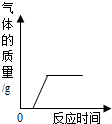 在久置的NaOH溶液中滴加盐酸 | |
| B. |  锌加入足量的稀硫酸中 | |
| C. |  往Na2SO4和HCl的混合溶液中加入Ba(OH)2溶液 | |
| D. |  向pH=9的NaOH溶液中不断加水 |
