题目内容
15.如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图.试回答下列问题:
(1)钠元素的原子序数为11;A、B、C中属于同种元素的粒子是BC;
(2)A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质;
(3)钠元素和氯元素形成的化合物是由离子(填“分子”、“原子”、“离子”)构成的.
分析 (1)根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同,据此进行分析解答.
(2)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,据此进行分析解答.
(3)钠元素和氯元素形成的化合物是氯化钠,据此进行分析解答.
解答 解:(1)根据元素周期表中的一格可知,左上角的数字为11,该元素的原子序数为11;元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,BC的质子数相同,属于同种元素.
(2)最外层电子数相同的元素化学性质相似,A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
(3)钠元素和氯元素形成的化合物是氯化钠,氯化钠是由钠离子和氯离子构成的.
故答案为:(1)11;BC;(2)最外层电子数;(3)离子.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.

练习册系列答案
相关题目
3.物质的性质决定其用途.下列物质的用途与性质对应关系错误的是( )
| A. | 氢气用作燃料----氢气具有可燃性 | |
| B. | 氧化钙作食品干燥剂----氧化钙能与水反应 | |
| C. | 氮气用作保护气----氮气化学性质稳定 | |
| D. | 干冰用于人工降雨----二氧化碳能与碱反应 |
10.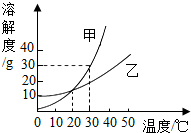 某固体物质在甲、乙两种溶剂中的溶解度曲线如右图所示.下列说法正确的是( )
某固体物质在甲、乙两种溶剂中的溶解度曲线如右图所示.下列说法正确的是( )
 某固体物质在甲、乙两种溶剂中的溶解度曲线如右图所示.下列说法正确的是( )
某固体物质在甲、乙两种溶剂中的溶解度曲线如右图所示.下列说法正确的是( )| A. | 该物质在甲中的溶解度比在乙中大 | |
| B. | 20℃时该物质在甲溶剂和乙溶剂中的质量分数相等 | |
| C. | 30℃时把20g该物质放入50g甲溶剂中,形成溶液的质量为65g | |
| D. | 40℃时该物质在甲、乙两种溶剂中形成等质量的饱和溶液降温至20℃,析出晶体的质量相等 |
20.酸雨,是目前人类遇到的全球性区域灾难之一.煤燃烧产生的SO2气体是形成酸雨的主要污染物,原因是SO2能与水结合生成弱酸性亚硫酸(H2SO3).
【查阅资料】①H2SO3易分解生成H2O和SO2②H2SO3和SO2都能使红色的品红溶液褪色.
③H2SO3、亚硫酸盐都易与空气中的氧气或稀硝酸反应生成H2SO4、硫酸盐.
④BaSO3不溶于水,可与盐酸、硫酸反应,BaSO3与酸的反应跟CaCO3与酸反应相似.
写出BaSO3与盐酸反应的化学方程式BaSO3+2HCl=BaCl2+SO2↑+H2O.
小刚同学利用酸碱中和反应的原理,向在空气中放置一段时间的酸雨(pH约为3)中加入足量的NaOH,并就反应后混合溶液中盐的成分进行如下探究:
【提出问题】反应后的混合溶液中盐的成分是什么?
【进行猜想】猜想1:只有Na2SO3; 猜想2:只有Na2SO4; 猜想3:既有Na2SO4,也有Na2SO3.
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、石灰水、品红溶液、石蕊溶液
【反思与交流】防止酸雨保护环境可采取的有效措施有少用煤做燃料.(写出其中一条)
【查阅资料】①H2SO3易分解生成H2O和SO2②H2SO3和SO2都能使红色的品红溶液褪色.
③H2SO3、亚硫酸盐都易与空气中的氧气或稀硝酸反应生成H2SO4、硫酸盐.
④BaSO3不溶于水,可与盐酸、硫酸反应,BaSO3与酸的反应跟CaCO3与酸反应相似.
写出BaSO3与盐酸反应的化学方程式BaSO3+2HCl=BaCl2+SO2↑+H2O.
小刚同学利用酸碱中和反应的原理,向在空气中放置一段时间的酸雨(pH约为3)中加入足量的NaOH,并就反应后混合溶液中盐的成分进行如下探究:
【提出问题】反应后的混合溶液中盐的成分是什么?
【进行猜想】猜想1:只有Na2SO3; 猜想2:只有Na2SO4; 猜想3:既有Na2SO4,也有Na2SO3.
【实验探究】限选试剂:稀硫酸、稀盐酸、稀硝酸、氯化钡溶液、石灰水、品红溶液、石蕊溶液
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 分别在A、B两只试管中各加入2mL反应后的混合溶液 | |
| 2 | 向A试管中滴加几滴品红溶液,再滴入足量的稀硫酸 | 有气泡产生,品红溶液褪色, 证明含有Na2SO3. |
| 3 | 向B试管中,加入足量的氯化钡溶液 | 再加入稀盐酸 ,证明含有Na2SO4,则猜想3成立. |
7.下列有关空气及其成分的说法,正确的是( )
| A. | 清新的空气是纯净物 | |
| B. | 氮气是空气中含量最多的气体,且能用来保存食品 | |
| C. | 氧气能跟很多物质反应,可以燃烧 | |
| D. | 稀有气体在生产和科研中用途不广 |
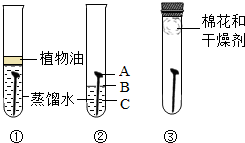 某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图所示:
某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图所示: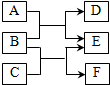 物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系.请回答下列问题(反应条件已略):
物质A~F都是初中化学中的常见物质,它们有如图所示的转化关系.请回答下列问题(反应条件已略):
