题目内容
在由碳元素和氧元素组成的混合气体中,碳元素和氧元素的质量比为1:2,则该气体的可能组成是
C0、CO2
C0、CO2
、CO、O2
CO、O2
、C0、O2、CO2
C0、O2、CO2
.分析:根据混合气体中含有C、O元素,先计算CO和CO2中C与O元素的质量比,根据混合气体中碳、氧两种元素的质量比为1:2分析其组成.
解答:解:根据混合气体中含有C、O元素,假设气体全为CO,则CO中C、O元素的质量比为12:16=3:4,假设气体全为CO2,则CO2中C、O元素的质量比为12:16×2=3:8,
由混合气体中碳、氧两种元素的质量比为1:2,3:8<1:2<3:4,则混合气体可能为C0、CO2,
又因为氧气中不含碳元素,氧气的存在只能够使C与O元素的质量比的数值变小,
则要满足混合气体中碳、氧两种元素的质量比为1:2,混合气体中必须含有CO,即气体也可能为CO、O2或CO、CO2、O2.
故答案为:C0、CO2;CO、O2;C0、O2、CO2.
由混合气体中碳、氧两种元素的质量比为1:2,3:8<1:2<3:4,则混合气体可能为C0、CO2,
又因为氧气中不含碳元素,氧气的存在只能够使C与O元素的质量比的数值变小,
则要满足混合气体中碳、氧两种元素的质量比为1:2,混合气体中必须含有CO,即气体也可能为CO、O2或CO、CO2、O2.
故答案为:C0、CO2;CO、O2;C0、O2、CO2.
点评:本题有一定难度,考查混合气体成分的确定,熟悉含C、O元素的气体、学会利用极限法和平均值法是解答本题的关键.

练习册系列答案
相关题目
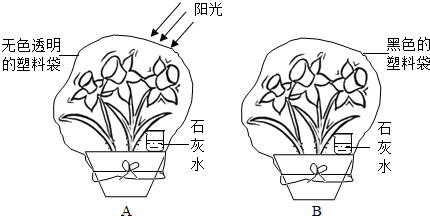 科学探究.
科学探究.
 某有机物在氧气中充分燃烧,产物只有二氧化碳和水.甲、乙两组同学分别用A、B两种方法测定它们的组成,得到两组数据(如图所示).
某有机物在氧气中充分燃烧,产物只有二氧化碳和水.甲、乙两组同学分别用A、B两种方法测定它们的组成,得到两组数据(如图所示).
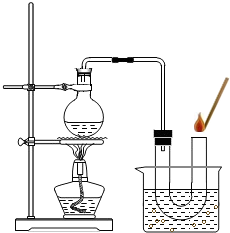 (1)碳酸钙的化学符号为
(1)碳酸钙的化学符号为