题目内容
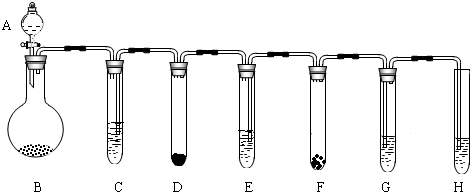
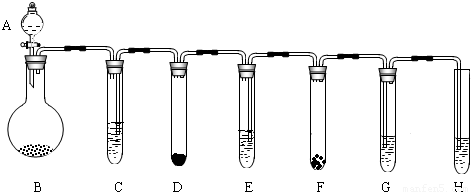
32、利用化学反应中气体产生的压力,可使多个化学反应依次发生,如图所示装置气密性良好,A~F各装置中盛放的物质分别为:
A.5%的双氧水 B.二氧化锰 C.稀硫酸
D.能溶于水的固体 E.浸有紫色石蕊溶液的棉花 F.无色溶液
将A中液体加入B中,关闭活塞,多个反应依次发生,D中有气泡产生,E中棉花呈红色.
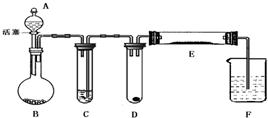
请回答下列问题:
(1)B中二氧化锰所起的作用是
(2)D中的固体是
(3)E中出现红色的原因是
(4)若要检验D中产生的气体仍有剩余,F中应盛放
A.5%的双氧水 B.二氧化锰 C.稀硫酸
D.能溶于水的固体 E.浸有紫色石蕊溶液的棉花 F.无色溶液
将A中液体加入B中,关闭活塞,多个反应依次发生,D中有气泡产生,E中棉花呈红色.

请回答下列问题:
(1)B中二氧化锰所起的作用是
催化作用
.(2)D中的固体是
碳酸钠
,发生反应的化学方程式为
Na2CO3+H2SO4=Na2 SO4+H2O+CO2↑
.(3)E中出现红色的原因是
二氧化碳与水反应生成碳酸,碳酸使紫色石蕊变红
.(4)若要检验D中产生的气体仍有剩余,F中应盛放
澄清石灰水
溶液,化学方程式为
Ca(OH)2+CO2═CaCO3↓+H2O
.分析:当打开A装置的活塞,B装置中会生成氧气,氧气产生的压力把C中的稀硫酸压入D中,与D物质反应,生成使石蕊试液变红的气体,这种气体应该是二氧化碳,由此可推出D物质是碳酸盐,并且能溶于水,可以是碳酸钠、碳酸钾等可溶性碳酸盐.检验二氧化碳是否有剩余,要用石灰水,根据是否变浑浊判断.
解答:解:(1)二氧化锰能加速双氧水分解,起催化作用.
(2)D中的固体能溶于水,能和稀硫酸反应生成二氧化碳气体,所以D是一种可溶性碳酸盐.
(3)E中出现红色的原因是D中生成的二氧化碳与石蕊试液中的水反应生成碳酸,碳酸使石蕊变红.
(4)因为D中生成的气体是二氧化碳,若要检验它是否仍有剩余,F中的液体就是石灰水,如果变浑浊说明有剩余.
答案(1) 催化作用.
(2 碳酸钠,Na2CO3+H2SO4=Na2 SO4+H2O+CO2↑
(3)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊变红.
(4) 澄清石灰水 Ca(OH)2+CO2═CaCO3↓+H2O
(2)D中的固体能溶于水,能和稀硫酸反应生成二氧化碳气体,所以D是一种可溶性碳酸盐.
(3)E中出现红色的原因是D中生成的二氧化碳与石蕊试液中的水反应生成碳酸,碳酸使石蕊变红.
(4)因为D中生成的气体是二氧化碳,若要检验它是否仍有剩余,F中的液体就是石灰水,如果变浑浊说明有剩余.
答案(1) 催化作用.
(2 碳酸钠,Na2CO3+H2SO4=Na2 SO4+H2O+CO2↑
(3)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊变红.
(4) 澄清石灰水 Ca(OH)2+CO2═CaCO3↓+H2O
点评:本题综合考查了氧气的制取,二氧化碳的制取及化学性质的验证,又注重了化学方程式是考查,是一道不错是试题.

练习册系列答案
相关题目