题目内容
19.将16g氧化铁固体放入147g稀硫酸中,恰好完全反应.试计算:(1)可生成硫酸铁多少克?
(2)所用硫酸的溶质质量分数是多少?
分析 氧化铁和稀硫酸反应生成硫酸铁和水,根据氧化铁的质量可以计算反应的硫酸的质量和生成的硫酸铁的质量,进一步可以计算稀硫酸中溶质的质量分数.
解答 解:设稀硫酸中溶质的质量为x,生成的硫酸铁质量为y,
Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,
160 294 400
16g x y
$\frac{160}{16g}=\frac{294}{x}$,$\frac{160}{16g}=\frac{400}{y}$
x=29.4g,y=40g,
稀硫酸中溶质的质量分数为$\frac{29.4g}{147g}$×100%=20%,
答案:
(1)40g
(2)20%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
9.电解质溶液不显电性是因为它的溶液里一定相等的是( )
| A. | 阴、阳离子所带的电荷总数 | B. | 阴、阳离子个数 | ||
| C. | 每个阴、阳离子所带的电荷数 | D. | 阴、阳离子所带的核电荷总数 |
10.下列四个图象,分别对应四种操作过程,其中正确的是( )
| A. | 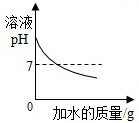 向氢氧化钠溶液中加入足量水稀释 | |
| B. | 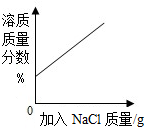 某温度下,向接近饱和的氯化钠溶液中加入氯化钠晶体 | |
| C. | 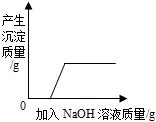 向氯化铁和盐酸的混合溶液中加入过量氢氧化钠溶液 | |
| D. | 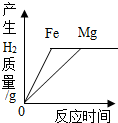 向两份同体积和相同质量分数的盐酸溶液中分别加入足量的铁粉和镁粉 |
7.今年入春至四月中旬,沈阳旱情严重,政府组织开展了较多的人工降雨活动.下列物质可用于人工降雨的是( )
| A. | 食盐 | B. | 干冰 | C. | 碳酸钠 | D. | 氯化钾 |
14.丙烷完全燃烧的反应可表示为:C3Hx+yO2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O,其中x、y的数值分别是( )
| A. | 8、5 | B. | 6、6 | C. | 5、7 | D. | 3、3 |
4.向含CaCl2、HCl二种溶质的溶液中加入10%的Na2CO3溶液实验过程中,加入Na2CO3溶液与产生沉淀或气体的关系如图1所示,加入Na2CO3溶液与溶液PH值变化如图2所示,则下列说法正确的是( )
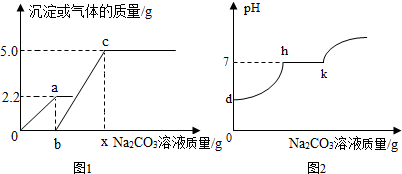

| A. | 图1中b→c段表示生成气体的过程 | |
| B. | 图1中b点的值为106 | |
| C. | 图1中c时溶液中有二种溶质 | |
| D. | 图1中0→a段反应过程中溶液PH值变化过程可用图2中d→h段表示 |
11.下列实验操作正确的是( )
| A. |  过滤 | B. |  闻气味 | C. |  稀释浓硫酸 稀释浓硫酸 | D. |  倾倒液体 倾倒液体 |
6.下列说法不符合事实的是( )
| A. | 钢铁生锈是缓慢氧化 | |
| B. | 铁锈的主要成分是四氧化三铁 | |
| C. | 铁在氧气中燃烧生成四氧化三铁 | |
| D. | 及时擦干被雨水淋湿的自行车可防止自行车生锈 |