题目内容
如图是几种实验室制取气体的发生装置与收集装置.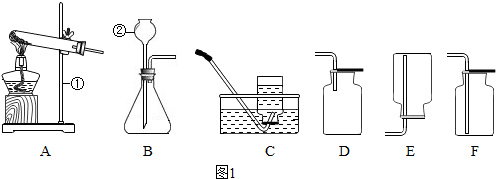
(1)写出图1中有标号的仪器名称:① ② .
(2)若用氯酸钾制取氧气时,所选用的发生装置是 (填字母序号,下同),收集装置是C或 ,该反应的化学方程式为 .
(3)若用C装置收集氧气,正确的操作顺序为 (填编号).
a.将导管伸入集气瓶口,让气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面
(4)选用B装置来制取氧气时,小明是“将二氧化锰加入装有过氧化氢溶液的锥形瓶中”,小亮是“把过氧化氢溶液缓缓加入盛有少量二氧化锰的锥形瓶中”,为得到平稳的氧气流 (填小明或小亮)的操作更好,该反应的化学方程式为 .实验结束后,若要分离出二氧化锰,可将残留物经过滤、洗涤、干燥.过滤操作时,需将圆形滤纸折叠.下列滤纸折叠过程图示2中,正确的是 (选填“甲”或“乙”).
甲:A→B→C 乙:A→B→D
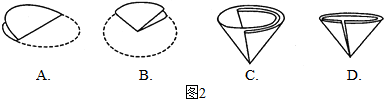
在过滤操作中玻璃棒的作用是 .若滤液仍浑浊,下列可能的原因有 .
A.滤纸破了 B.滤纸没有紧靠漏斗内壁
C.承接滤液的烧杯没洗干净 D.漏斗中液体的液面高于滤纸边缘
(5)图3是“铁丝在氧气中燃烧”实验的改进装置.实验时,打开分夜漏斗活塞,通入干燥氧气约10秒,引燃铁丝下端火柴杆,伸入塑料瓶内,并对准玻璃管口正上方,观察到的现象是:铁丝剧烈燃烧, ;该反应的化学方程式为 .改进后装置具有的优点是 (填序号).
①氧气无需提前制备和收集,操作更方便
②塑料瓶代替集气瓶,防止集气瓶炸裂,更安全
③装置集氧气的制取、干燥和性质验证于一体,实验更优化
(6)取31.6g高锰酸钾,加热一段时间后停止,共收集到1.6g氧气.
①参加反应的高锰酸钾的质量是多少?(写出详细解题过程) 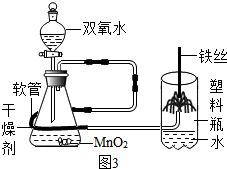
②剩余固体中氧元素的质量分数为 .(此空直接填写结果,计算结果保留到0.1%)
③有同学发现,不慎将高锰酸钾粘到了手上,会留下一时洗不掉的褐色斑痕.老师说,这是高锰酸钾氧化作用对皮肤的腐蚀所致.针对这个案例,在实验前你想提醒同学们注是 .

(1)写出图1中有标号的仪器名称:①
(2)若用氯酸钾制取氧气时,所选用的发生装置是
(3)若用C装置收集氧气,正确的操作顺序为
a.将导管伸入集气瓶口,让气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面
(4)选用B装置来制取氧气时,小明是“将二氧化锰加入装有过氧化氢溶液的锥形瓶中”,小亮是“把过氧化氢溶液缓缓加入盛有少量二氧化锰的锥形瓶中”,为得到平稳的氧气流
甲:A→B→C 乙:A→B→D

在过滤操作中玻璃棒的作用是
A.滤纸破了 B.滤纸没有紧靠漏斗内壁
C.承接滤液的烧杯没洗干净 D.漏斗中液体的液面高于滤纸边缘
(5)图3是“铁丝在氧气中燃烧”实验的改进装置.实验时,打开分夜漏斗活塞,通入干燥氧气约10秒,引燃铁丝下端火柴杆,伸入塑料瓶内,并对准玻璃管口正上方,观察到的现象是:铁丝剧烈燃烧,
①氧气无需提前制备和收集,操作更方便
②塑料瓶代替集气瓶,防止集气瓶炸裂,更安全
③装置集氧气的制取、干燥和性质验证于一体,实验更优化
(6)取31.6g高锰酸钾,加热一段时间后停止,共收集到1.6g氧气.
①参加反应的高锰酸钾的质量是多少?(写出详细解题过程)

②剩余固体中氧元素的质量分数为
③有同学发现,不慎将高锰酸钾粘到了手上,会留下一时洗不掉的褐色斑痕.老师说,这是高锰酸钾氧化作用对皮肤的腐蚀所致.针对这个案例,在实验前你想提醒同学们注是
考点:氧气的制取装置,过滤的原理、方法及其应用,氧气的化学性质,氧气的收集方法,制取氧气的操作步骤和注意点,根据化学反应方程式的计算
专题:有关化学方程式的计算,常见气体的实验室制法、检验、干燥与净化
分析:(1)根据仪器名称解答;
(2)根据反应物的状态和反应条件决定发生装置,气体的物理性质决定收集装置;
(3)根据实验的注意事项和顺序解答;
(4)根据过氧化氢制取氧气的原理和注意事项,以及过滤的注意事项分析解答;
(5)根据铁丝在氧气中燃烧现象,反应原理,装置的特点分析;
(6)①根据氧气的质量结合化学方程式即可计算高锰酸钾的质量;
②根据高锰酸钾中氧元素的质量减去生成氧气的质量除以剩余固体的质量,即可解答;
③根据药品使用注意事项解答;
(2)根据反应物的状态和反应条件决定发生装置,气体的物理性质决定收集装置;
(3)根据实验的注意事项和顺序解答;
(4)根据过氧化氢制取氧气的原理和注意事项,以及过滤的注意事项分析解答;
(5)根据铁丝在氧气中燃烧现象,反应原理,装置的特点分析;
(6)①根据氧气的质量结合化学方程式即可计算高锰酸钾的质量;
②根据高锰酸钾中氧元素的质量减去生成氧气的质量除以剩余固体的质量,即可解答;
③根据药品使用注意事项解答;
解答:解:(1)仪器①为铁架台; ②为长颈漏斗;
(2)若用氯酸钾制取氧气时,应选择加热固体产生气体的发生装置A;由于氧气的密度比空气大,不易溶于水;应选择排水法或向上排空气法收集;
氯酸钾在二氧化锰催化和加热条件下生成氯化钾和氧气;
(3)排水法收集时应按b.将装满水的集气瓶倒置在水槽中;a.将导管伸入集气瓶口,让气体进入瓶中;c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面,的顺序操作;
(4)为得到平稳的氧气流应把过氧化氢溶液缓缓加入盛有少量二氧化锰的锥形瓶中;过氧化氢在二氧化锰的催化下分解生成水和氧气;过滤时应把叠好的滤纸分成一边三层一边一层进行过滤;
(5)铁丝在氧气中燃烧的现象是铁丝剧烈燃烧,火星四射,放出热量,生成黑色固体;反应的化学方程式为:3Fe+2O2
Fe3O4;改进后装置①氧气无需提前制备和收集,操作更方便;②塑料瓶代替集气瓶,防止集气瓶炸裂,更安全;③装置集氧气的制取、干燥和性质验证于一体,实验更优化.
(6))①解:设参加反应的高锰酸钾的质量为x,
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 1.6g
=
x=15.8g
答:参加反应的高锰酸钾的质量为15.8g.
(2)剩余固体中氧元素的质量分数为:
×100%=37.3%;
(3)高锰酸钾氧化作用对皮肤有腐蚀作用,在实验前你想提醒同学们注是避免药品与皮肤直接接触.
答案:
(1)①铁架台; ②长颈漏斗;
(2)A;F;
(3)bac
(4)小亮 2H2O2
2H2O+O2↑ 甲 引流 ACD
(5)火星四射,放出热量,生成黑色固体; 3Fe+2O2
Fe3O4; ①②③;
(6)①解:设参加反应的高锰酸钾的质量为x,
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 1.6g
=
x=15.8g
答:参加反应的高锰酸钾的质量为15.8g.
②37.3%; ③避免药品与皮肤直接接触.
(2)若用氯酸钾制取氧气时,应选择加热固体产生气体的发生装置A;由于氧气的密度比空气大,不易溶于水;应选择排水法或向上排空气法收集;
氯酸钾在二氧化锰催化和加热条件下生成氯化钾和氧气;
(3)排水法收集时应按b.将装满水的集气瓶倒置在水槽中;a.将导管伸入集气瓶口,让气体进入瓶中;c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面,的顺序操作;
(4)为得到平稳的氧气流应把过氧化氢溶液缓缓加入盛有少量二氧化锰的锥形瓶中;过氧化氢在二氧化锰的催化下分解生成水和氧气;过滤时应把叠好的滤纸分成一边三层一边一层进行过滤;
(5)铁丝在氧气中燃烧的现象是铁丝剧烈燃烧,火星四射,放出热量,生成黑色固体;反应的化学方程式为:3Fe+2O2
| ||
(6))①解:设参加反应的高锰酸钾的质量为x,
2KMnO4
| ||
316 32
x 1.6g
| 316 |
| x |
| 32 |
| 1.6g |
x=15.8g
答:参加反应的高锰酸钾的质量为15.8g.
(2)剩余固体中氧元素的质量分数为:
31.6g×
| ||
| 31.6g-1.6g |
(3)高锰酸钾氧化作用对皮肤有腐蚀作用,在实验前你想提醒同学们注是避免药品与皮肤直接接触.
答案:
(1)①铁架台; ②长颈漏斗;
(2)A;F;
(3)bac
(4)小亮 2H2O2
| ||
(5)火星四射,放出热量,生成黑色固体; 3Fe+2O2
| ||
(6)①解:设参加反应的高锰酸钾的质量为x,
2KMnO4
| ||
316 32
x 1.6g
| 316 |
| x |
| 32 |
| 1.6g |
x=15.8g
答:参加反应的高锰酸钾的质量为15.8g.
②37.3%; ③避免药品与皮肤直接接触.
点评:本题考查了学生对实验室制取气体的反应原理、装置选取、仪器使用等知识,能较好培养学生解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
用分子的观点解释下列事实,其中不正确的是( )
| A、水沸腾后壶盖被顶起-温度升高,分子的体积变大 |
| B、春天百花盛开,花香四溢-分子在不断运动 |
| C、50mL水与50mL酒精混合,液体总体积小于100 mL-分子之间有间隔 |
| D、水与过氧化氢化学性质不同-分子构成不同 |
下列是日常生活中发生的变化,其中发生了化学变化的是( )
| A、水受热沸腾 | B、铁锅生锈 |
| C、桔子榨成汁 | D、玻璃破碎 |
用下列装置进行实验,不能达到实验目的是( )
A、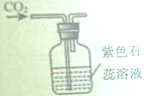 验证CO2性质 |
B、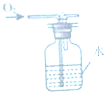 监控气体流速 |
C、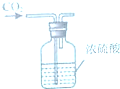 干燥CO2 |
D、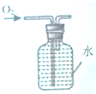 收集O2 |
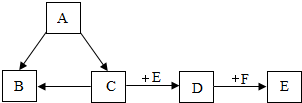 如图是A、B、C、D、E、F六种物质问的关系(“→”表示物质间的转化关系,部分反应条件和生成物省略).A、B、D是氧化物,且A、B为无色液体,C、E、F是单质,D、F为黑色固体.
如图是A、B、C、D、E、F六种物质问的关系(“→”表示物质间的转化关系,部分反应条件和生成物省略).A、B、D是氧化物,且A、B为无色液体,C、E、F是单质,D、F为黑色固体.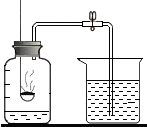 已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示: