题目内容
14.小雪同学想测定某Cu-Ag合金中两种金属的质量比.称取这种合金9.6g,加入足量AgNO3溶液充分反应后过滤,将所得固体洗涤、干燥后称量.并绘制成图.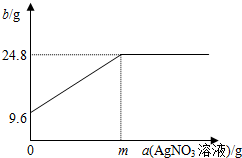
(1)反应后烧杯中银的质量24.8g
(2)计算该合金中铜的质量.
分析 (1)根据表中的数据分析反应后烧杯中银的质量;
(2)根据铜和硝酸银反应生成硝酸铜和银,依据固体增加的质量计算合金中铜的质量.
解答 解:(1)反应后烧杯中银的质量是24.8g;
(2)设该合金中铜的质量为x
Cu+2AgNO3=Cu(NO3)2+2Ag 固体质量增加
64 216 216-64=152
x 24.8g-9.6g=15.2g
$\frac{64}{x}$=$\frac{152}{15.2g}$
x=6.4g
故答案为:(1)24.8g;
(2)6.4g.
点评 本题属一道综合计算题,涉及到化学方程式及溶液的计算,解题的关键是对问题进行深入的探讨与分析,从而确定反应时量的关系,从难度上讲应该属于竞赛题系列.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
7.图1是锂原子的构成示意图,根据图示信息回答下列问题:
(1)锂元素的原子序数为3,元素符号为Li.
(2)锂原子的结构示意图为图2中的D(填字母).

(3)锂元素与氧元素形成的化合物的化学式为Li2O.
(1)锂元素的原子序数为3,元素符号为Li.
(2)锂原子的结构示意图为图2中的D(填字母).

(3)锂元素与氧元素形成的化合物的化学式为Li2O.
5.下列有关酸和碱的说法错误的是( )
| A. | 稀硫酸滴到纸张上,在水分挥发的过程中硫酸的浓度增大也会使纸张逐渐炭化 | |
| B. | 被蚂蚁、蚊子叮咬了,涂上稀氨水或肥皂水可以止痛、消炎 | |
| C. | 配制氢氧化钠溶液时氢氧化钠固体可放在称量纸上称量 | |
| D. | 用氢氧化钠制作叶脉书签是利用了氢氧化钠的腐蚀性 |
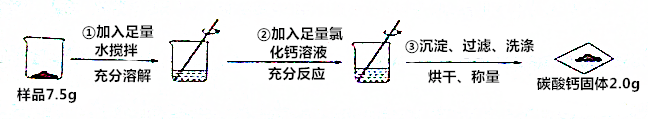
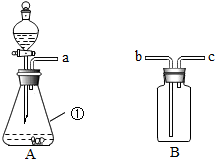 如图所示的装置适当组合可用于O2、CO2等气体的制取.
如图所示的装置适当组合可用于O2、CO2等气体的制取.