题目内容
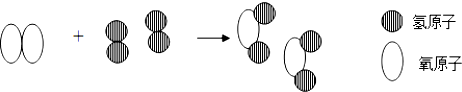
11.由分子构成的物质,分子是保持化学性质的最小粒子;原子是化学变化中的最小粒子.分析 根据分子的构成以及分子和原子的概念来分析解答.
解答 解:原子构成的分子,分子是保持物质化学性质的最小粒子,原子在化学变化中不能再分,是化学变化中的最小粒子.
故填:化学性质;化学变化中.
点评 明确物质的构成,分子、原子的概念是解题的关键.

练习册系列答案
相关题目
1.下列鉴别物质的方法中,切实可行的是( )
| A. | 用酚酞溶液鉴别NaCl溶液和盐酸 | |
| B. | 用燃着的木条鉴别CO2和N2 | |
| C. | 用紫色石蕊溶液鉴别稀盐酸和稀硫酸 | |
| D. | 用紫色石蕊溶液鉴别NaOH和稀盐酸 |
6.在实验室中,下列有错的是( )
| A. | 在演示实验和分组实验中,要力求利用最少的实验用品,获得最佳的实验效果,最大 限度的减少废弃物 | |
| B. | 给试管里的液体加热时,不要把拇指按在试管夹短柄上,试管口不能对着自己,试管 内液体不超过试管容积的一半 | |
| C. | 取用液体药品时,要把瓶塞倒放在桌面上,标签朝向手心,放回原处时标签向外 | |
| D. | 不能用手接触实验室里的药品,不要凑到容器口闻气体的气味,不能尝药品的味道 |