题目内容
乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属.乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二: ;猜想三:Ca(OH)2.
【交流反思】经过同学们交流讨论,认为猜想一不成立.否定猜想一的理由是: .
【进行试验】
【实验结论】碳化钙与水反应的化学方程式为:
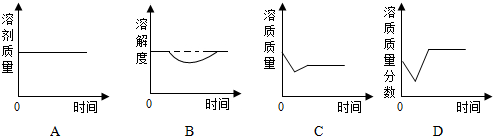
【拓展】某温度时,向一定量的饱和石灰水中加放少量生石灰,再恢复到原来温度,下列相关图象描述正确的是 .
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO;猜想二:
【交流反思】经过同学们交流讨论,认为猜想一不成立.否定猜想一的理由是:
【进行试验】
| 实验操作 | 实验现象 | 结论 | |
| 实验一 | 取样于试管中,滴加 | 没气泡 | 猜想二不成立 |
| 实验二 | 取少量白色固体加水溶解,静置后取上层清液,通入二氧化碳气体 | 猜想三成立 |
【拓展】某温度时,向一定量的饱和石灰水中加放少量生石灰,再恢复到原来温度,下列相关图象描述正确的是

考点:实验探究物质的组成成分以及含量,生石灰的性质与用途,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【做出猜想】根据质量守恒定律的元素守恒可知,白色固体可能是氧化钙,或碳酸钙,或氢氧化钙;
【交流反思】氧化钙能和水反应生成氢氧化钙;
【进行实验】碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能使澄清的石灰水变浑浊;
【实验结论】碳化钙和水反应生成了乙炔和氢氧化钙,可以据此写出该反应的化学方程式
【拓展】虽然生石灰遇水会放出大量热而使饱和溶液溶液升高,但题中明确“恢复到原来的温度”,因此在分析本问题时不需要考虑温度对溶液的影响;由于氧化钙能与水发生反应生成氢氧化钙,易被误解为增加了溶液中的溶质,其实是氧化钙反应消耗了饱和溶液中的水,而使饱和溶液因减少溶剂水而析出固体,饱和溶液的溶质、溶剂质量同时减少,溶液仍为饱和溶液.
【交流反思】氧化钙能和水反应生成氢氧化钙;
【进行实验】碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能使澄清的石灰水变浑浊;
【实验结论】碳化钙和水反应生成了乙炔和氢氧化钙,可以据此写出该反应的化学方程式
【拓展】虽然生石灰遇水会放出大量热而使饱和溶液溶液升高,但题中明确“恢复到原来的温度”,因此在分析本问题时不需要考虑温度对溶液的影响;由于氧化钙能与水发生反应生成氢氧化钙,易被误解为增加了溶液中的溶质,其实是氧化钙反应消耗了饱和溶液中的水,而使饱和溶液因减少溶剂水而析出固体,饱和溶液的溶质、溶剂质量同时减少,溶液仍为饱和溶液.
解答:解:【做出猜想】反应物为碳化钙(块状固体,化学式为CaC2)与水,根据质量守恒定律的元素守恒可知:猜想一:CaO;猜想二CaCO3;猜想三:Ca(OH)2.
【交流反思】经过同学们交流讨论,认为猜想一CaO不成立.否定猜想一的理由是:CaO能与水反应.
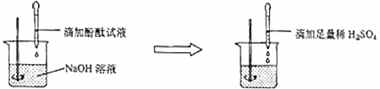
【进行实验】(一)根据碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;所以可以取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡放出,则证明猜想二不成立.
(二)根据二氧化碳能使澄清的石灰水变浑浊;则取少量白色固体加入到水中,取上层清液,通入二氧化碳气体,有白色沉淀出现,证明猜想三成立.
【实验结论】碳化钙和水反应生成了乙炔和氢氧化钙,该反应的化学方程式为:CaC2+2H2O═C2H2↑+Ca(OH)2;
【拓展】A、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,故A错误;
B、固体物质的溶解度只受温度的影响,由于溶液的温度不变,因此,溶质的溶解度也不变,故B错误;
C、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,饱和溶液的溶剂减少会造成溶质析出,所以溶质减少,故C错误;
D、加入氧化钙后,氧化钙和水反应放出热量,而氢氧化钙的溶解度随温度的升高而降低,所以溶液中溶质的质量分数下降,当恢复到原温度时,根据相同温度下的同种溶质的饱和溶液的溶质质量分数相同,饱和溶液的溶质质量分数不变,故D正确;
故选D.
故答案为:【做出猜想】CaCO3;
【交流反思】CaO能与水反应.
【进行试验】
【实验结论】CaC2+2H2O═C2H2↑+Ca(OH)2;
【拓展】D.
【交流反思】经过同学们交流讨论,认为猜想一CaO不成立.否定猜想一的理由是:CaO能与水反应.
【进行实验】(一)根据碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;所以可以取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡放出,则证明猜想二不成立.
(二)根据二氧化碳能使澄清的石灰水变浑浊;则取少量白色固体加入到水中,取上层清液,通入二氧化碳气体,有白色沉淀出现,证明猜想三成立.
【实验结论】碳化钙和水反应生成了乙炔和氢氧化钙,该反应的化学方程式为:CaC2+2H2O═C2H2↑+Ca(OH)2;
【拓展】A、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,故A错误;
B、固体物质的溶解度只受温度的影响,由于溶液的温度不变,因此,溶质的溶解度也不变,故B错误;
C、由于氧化钙与饱和溶液中的水发生反应而使溶液因此减少了水,饱和溶液的溶剂减少会造成溶质析出,所以溶质减少,故C错误;
D、加入氧化钙后,氧化钙和水反应放出热量,而氢氧化钙的溶解度随温度的升高而降低,所以溶液中溶质的质量分数下降,当恢复到原温度时,根据相同温度下的同种溶质的饱和溶液的溶质质量分数相同,饱和溶液的溶质质量分数不变,故D正确;
故选D.
故答案为:【做出猜想】CaCO3;
【交流反思】CaO能与水反应.
【进行试验】
| 实验操作 | 实验现象 | 结论 | |
| 实验一 | 取样于试管中,滴加 稀盐酸 | 没气泡 | 猜想二不成立 |
| 实验二 | 取少量白色固体加水溶解,静置后取上层清液,通入二氧化碳气体 | 产生白色沉淀 | 猜想三成立 |
【拓展】D.
点评:化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.

练习册系列答案
相关题目
2014年1月底,浙江、上海、广东等地相继发现人感染H7N9病毒,帕拉米韦是一种新型的抗流感病毒药物,其化学式为C15H28N4O4.有关帕拉米韦的说法正确的是( )
| A、帕拉米韦中氮元素与氧元素的质量比为14:8 |
| B、帕拉米韦属于氧化物 |
| C、帕拉米韦由碳、氢、氮、氧四种元素组成 |
| D、帕拉米韦分子中氢、氮原子的个数比15:4 |
 化学基础知识是学好化学的关键,请按下列要求填空.
化学基础知识是学好化学的关键,请按下列要求填空.