题目内容
结合下列与铁有关的实验,回答问题:
(1)A实验中为避免炸裂集气瓶底,实验前应采取的措施是 ;
(2)B实验中发生的反应可用化学方程式表示为 ;
(3)C实验中能够在铁丝表面观察到的明显现象是 ;
(4)D实验的目的是 .

(1)A实验中为避免炸裂集气瓶底,实验前应采取的措施是
(2)B实验中发生的反应可用化学方程式表示为
(3)C实验中能够在铁丝表面观察到的明显现象是
(4)D实验的目的是
考点:金属的化学性质,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)细铁丝在纯氧气中燃烧时,为了防止铁的熔化物温度过高而炸裂集气瓶,应该在瓶底放少量水或细沙.
(2)根据反应物、生成物和条件书写方程式.
(3)根据铁与硫酸铜反应分析.
(4)D实验探究铁生锈的条件.
(2)根据反应物、生成物和条件书写方程式.
(3)根据铁与硫酸铜反应分析.
(4)D实验探究铁生锈的条件.
解答:解:(1)细铁丝在纯氧气中燃烧时,为了防止铁的熔化物温度过高而炸裂集气瓶,应该在瓶底放少量水或细沙.
(2)铁与盐酸反应生成氯化亚铁和水,方程式为Fe+2HCl=FeCl2+H2↑.
(3)铁与硫酸铜反应现象为:铁丝表面有有红色物质附着,溶液由蓝色变浅绿色.
(4)D实验通过abc对照来探究铁生锈的条件
故答案为:(1)事先在瓶内放少量水或细沙;
(2)Fe+2HCl═FeCl2+H2↑(化学式0.(5分),配平和“↑”0.(5分),化学式得0分);
(3)有红色物质附着;
(4)探究铁生锈的条件.
(2)铁与盐酸反应生成氯化亚铁和水,方程式为Fe+2HCl=FeCl2+H2↑.
(3)铁与硫酸铜反应现象为:铁丝表面有有红色物质附着,溶液由蓝色变浅绿色.
(4)D实验通过abc对照来探究铁生锈的条件
故答案为:(1)事先在瓶内放少量水或细沙;
(2)Fe+2HCl═FeCl2+H2↑(化学式0.(5分),配平和“↑”0.(5分),化学式得0分);
(3)有红色物质附着;
(4)探究铁生锈的条件.
点评:本题为基础性考查.书写化学方程式时,要注意配平.金属的性质是中考的重要考点之一,一定要加强记忆,理解应用,本考点一般出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组物质,按单质、化合物、混合物顺序排列的是( )
| A、液态氧、蒸馏水、透明的河水 |
| B、稀有气体、氯化氢气体、液化石油气 |
| C、固态氮、干冰、冰水共存物 |
| D、天然气、煤、石油 |
对实验现象的分析,有助于我们理解科学本质.下列根据实验现象得出的结论正确的是( )
| A、某固体溶于水放出热量,说明该固体一定是氢氧化钠 |
| B、将燃着的木条伸入某气体中,木条火焰熄灭,则该气体一定是二氧化碳 |
| C、将氯化钡溶液滴加到某无色溶液中,产生不溶于稀硝酸的白色沉淀,则该溶液中一定含有硫酸根离子 |
| D、将干冷静的烧杯罩在某气体燃烧的火焰上方,烧杯内壁出现小水珠,说明该气体中一定含有氢元素 |
下列图象中错误的是( )
A、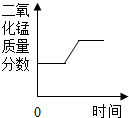 表示KClO3和MnO2加热制氧气过程中MnO2的质量分数 |
B、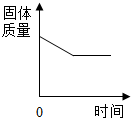 表示CO还原CuO的实验中,试管内的固体质量与时间的关系图 |
C、 表示向CaCl2(含少量HCl)溶液中滴加K2CO3溶液,CaCl2与加入K2CO3的量关系图 |
D、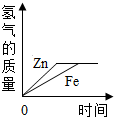 表示等质量、相同质量分数的稀硫酸与足量的铁片和锌片反应 |
 如图所示:先打开a,可观察到的现象是:
如图所示:先打开a,可观察到的现象是: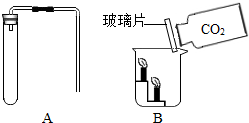 化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.
化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.
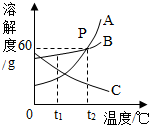 如图为A、B、C三种固体物质的溶解度曲线,根据图示完成下列问题:
如图为A、B、C三种固体物质的溶解度曲线,根据图示完成下列问题: