题目内容
19.今有未知溶质质量分数的稀盐酸50g,与6.5g锌恰好完全反应后,(1)产生氢气的质量.
(2)所用稀盐酸中溶质的质量分数.
分析 由锌和稀盐酸的质量根据锌与盐酸反应的化学方程式可以计算出稀盐酸中溶质的质量分数和氢气的质量;
解答 解:设稀盐酸中溶质的质量分数为x.生成氢气的质量是y
Zn+2HCl=ZnCl2+H2↑
65 73 2
6.5g 50g×x y
$\frac{65}{6.5g}=\frac{73}{50g×x}=\frac{2}{y}$
x=14.6% y=0.2g
答:(1)生成氢气的质量是0.2g;(2)稀盐酸中溶质的质量分数为14.6%,
点评 本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用题,题型基础难度不大.

练习册系列答案
相关题目
4.下列有关事实不能用金属活动性顺序解释的是( )
| A. | 不能用金属铜与稀硫酸反应制取氢气 | |
| B. | 铜能将银从硝酸银溶液中置换出来 | |
| C. | 镁和铝与稀盐酸反应的剧烈程度不同 | |
| D. | 银的导电性强于铜 |
5.下列反应既是化合反应,又是氧化反应的是( )
| A. | 甲烷+氧气$\stackrel{点燃}{→}$ 二氧化碳+水 | |
| B. | 磷+氧气$\stackrel{点燃}{→}$ 五氧化磷 | |
| C. | 氨气+氯化氢→氯化铵 | |
| D. | 氯酸钾 $→_{△}^{二氧化锰}$ 氯化钾+氧气 |
14. 某化肥说明书的一部分如图所示.
某化肥说明书的一部分如图所示.
(1)该化肥的化学性质为:①与碱性物质混用会因放出氨气,而损失肥效; ②受热易分解,
(2)该化肥的物理性质为易溶于水.
(3)一包该化肥(50kg)中有8kg氮元素.
 某化肥说明书的一部分如图所示.
某化肥说明书的一部分如图所示.(1)该化肥的化学性质为:①与碱性物质混用会因放出氨气,而损失肥效; ②受热易分解,
(2)该化肥的物理性质为易溶于水.
(3)一包该化肥(50kg)中有8kg氮元素.
8.下列物质的用途错误的是( )
| A. | 氢氧化钠用作食品干燥剂 | B. | 碳酸氢钠用于治疗胃酸过多症 | ||
| C. | 碳酸钙用于补钙 | D. | 氯化钠用于配制生理盐水 |
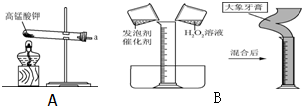 实验小组同学做了如下实验.
实验小组同学做了如下实验.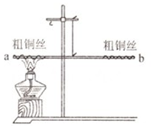 在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平(如图所示),然后用酒精灯加热数分钟,停止加热后冷却.写出观察到的现象左端铜丝表面变黑,玻璃棒左端下沉,玻璃棒右端上升,化学方程式是2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.产生这种现象的原因铜与空气中氧气发生反应生成氧化铜,质量增大.
在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平(如图所示),然后用酒精灯加热数分钟,停止加热后冷却.写出观察到的现象左端铜丝表面变黑,玻璃棒左端下沉,玻璃棒右端上升,化学方程式是2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.产生这种现象的原因铜与空气中氧气发生反应生成氧化铜,质量增大.