题目内容
3.化学实验中常常会出现意外情况,这是提升我们学科素养的良好机会,要根据具体情况区别对待,善于发现和解决问题.例如:用盐酸和碳酸钙固体反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.针对此现象,同学们提出了自己的想法和做法,请你帮助他们完成以下探究.【假设】小英的假设:澄清石灰水已变质 小青的假设:气体X中除了有CO2外,还有HCl
【实验探究】
Ⅰ.小英的探究:
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用 澄清石灰 水是否变 质 | ①用一支试管另取少量原澄清石灰水②取稀硫酸与碳酸钠 反应制取CO2 ③将产生的气体通入所用澄清石灰水中 | 步骤③中现象为: 石灰水变浑浊,或未变浑浊 | 步骤②中反应方程式为: H2SO4+Na2CO3=Na2SO4+H2O+CO2↑ 步骤③可能的反应方程式略 实验结论:所用澄清石灰水没有变质,或所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化.学方程式和实验结论 |
| 探究气体X中是否含有HCl气体 | 将气体X通入硝酸银溶液 | 有白色沉淀生成 | 反应方程式为:HCl+AgNO3=AgCl↓+HNO3 实验结论:气体X中含有HCl气体 |
Ⅲ.同学们经过讨论发现,只用一组实验装置就可以同时完成上述两个假设的探究.请你从下图中选择一组合理的装置A(填序号).
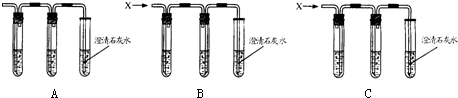
Ⅳ.在上述合理装置的第二支试管内应放入AgNO3溶液,其作用是验证HCl气体已经除尽.
分析 【假设】
盐酸中易挥发出氯化氢气体,氯化氢气体溶于水析出盐酸,盐酸能和碳酸钙反应生成氯化钙、水和二氧化碳;
【实验探究】
碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊;
稀盐酸能和硝酸银反应生成白色沉淀氯化银和硝酸;
【实验反思】
B、C装置中的导管进出不合理;
A中,第一个试管中应该加入饱和碳酸氢钠溶液,饱和碳酸氢钠溶液不能和二氧化碳反应,能和稀盐酸反应生成氯化钠、水和二氧化碳;
第二个试管中应该放入硝酸银溶液,用来检验氯化氢气体是否除尽.
解答 解:【假设】气体X中除了有CO2外,还有HCl.
故填:HCl.
【实验探究】
Ⅰ.小英的探究如下表所示:
| 实验目的 | 实验步骤 | 可能的实验现象 | 化学方程式和实验结沦 |
| 探究所用 澄清石灰 水是否变 质 | ①用一支试管另取少量原澄清石灰水②取稀硫酸与碳酸钠 反应制取CO2 ③将产生的气体通入所用澄清石灰水中 | 步骤③中现象为:石灰水变浑浊,或未变浑浊 | 步骤②中反应方程式为: H2SO4+Na2CO3=Na2SO4+H2O+CO2↑ 步骤③可能的反应方程式略 实验结论:所用澄清石灰水没有变质,或所用澄清石灰水已变质 |
| 实验目的 | 实验步骤 | 实验现象 | 化.学方程式和实验结论 |
| 探究气体X中是否含有HCl气体 | 将气体X通入硝酸银溶液 | 有白色沉淀生成 | 反应方程式为:HCl+AgNO3=AgCl↓+HNO3 实验结论:气体X中含有HCl气体 |
B、C装置中的导管进出不合理,不能用于探究实验;
A中,第一个试管中应该加入饱和碳酸氢钠溶液,饱和碳酸氢钠溶液不能和二氧化碳反应,能和稀盐酸反应生成氯化钠、水和二氧化碳;
第二个试管中应该放入硝酸银溶液,用来检验氯化氢气体是否除尽;
再通过观察澄清石灰水是否变浑浊,就可以确定澄清石灰水是否变质.
故填:A;AgNO3;验证HCl气体已经除尽.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
13.在人体含量最多的化学元素是( )
| A. | 碳 | B. | 氢 | C. | 氧 | D. | 钙 |
11.下列验证实验不能成功的是( )
| A. | 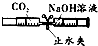 C02能与烧碱溶液反应 | B. |  不同物质的着火点不同 | ||
| C. |  分子在不断运动 | D. |  质量守恒定律 |
15.除去下列物质中的杂质所选用的试剂及操作方法正确的一组是( )
| 物 质 | 所含杂质 | 除 去 杂 质 的 方 法 | |
| A | KClO3 | 少量MnO2 | 加热 |
| B | N2气体 | (O2) | 将气体缓缓通过灼热的铜网 |
| C | Fe | (Cu) | 稀硫酸溶液、过滤 |
| D | CO2 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
12.下列化学肥料属于复合肥料的是( )
| A. | 尿素 CO(NH2)2 | B. | 重过磷酸钙 Ca(H2PO4)2 | ||
| C. | 氯化钾 KCl | D. | 磷酸二氢铵 NH4H2PO4 |
12.活性氧化锌用作橡胶硫化的活性剂、补强剂.以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下:
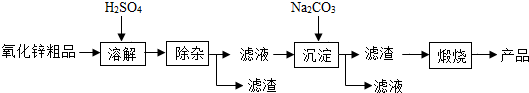
一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
(1)“溶解”前将氧化锌粗品粉碎成细颗粒,目的是增大接触面积,加快反应速率.
(2)“溶解”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+等杂质.先加入Na2CO3(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2.在氧化还原反应中,化合价升高的反应物叫还原剂,化合价降低的反应物叫氧化剂,那么KMnO4在该反应中作为氧化剂(填“还原剂”或“氧化剂”).
(3)杂质Cu2+可利用置换反应除去,应选择的试剂是锌.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450~500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.

一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
| pH | 3.2 | 6.7 | 8.0 | 9.7 |
(2)“溶解”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+等杂质.先加入Na2CO3(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2.在氧化还原反应中,化合价升高的反应物叫还原剂,化合价降低的反应物叫氧化剂,那么KMnO4在该反应中作为氧化剂(填“还原剂”或“氧化剂”).
(3)杂质Cu2+可利用置换反应除去,应选择的试剂是锌.
(4)“沉淀”得到ZnCO3•2Zn(OH)2•H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为ZnCO3•2Zn(OH)2•H2O$\frac{\underline{\;450~500℃\;}}{\;}$3ZnO+CO2↑+3H2O↑.