题目内容
4.下列有关氧气的“自述”,正确的是( )| A. | 在100g空气中我有21g | B. | 我能供给呼吸 | ||
| C. | 我具有可燃性 | D. | 通常情况下,我是淡蓝色的 |
分析 根据空气中氧气的体积分数和氧气的性质判断,氧气是无色的气体,具有助燃性,能供给呼吸.
解答 解:A、空气中大约含有21%的氧气是指100体积空气中含有21体积的氧气.故A错误;
B、氧气能供给呼吸,故B正确;
C、氧气具有助燃性,不具有可燃性.故C错误.
D、在通常状况下,氧气是无色无味的气体,故D错误.
故选B.
点评 本考点考查了空气中氧气的含量和氧气的性质,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
14.氢氧化钾是我国古代纺织业常用的洗涤剂,古人将贝壳(主要成分是碳酸钙)灼烧后的固体,与草木灰(主要成分是碳酸钾)在水中相互作用,生成氢氧化钾.在上述反应过程中没有涉及的化学反应基本类型是( )
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
15.下列说法不正确的是( )
| A. | 与氧气接触的物质都会发生缓慢氧化 | |
| B. | 单质、化合物、氧化物、酸、碱、盐都属于纯净物 | |
| C. | 敞口放置的浓盐酸和浓硫酸,其溶质质量分数都会减小 | |
| D. | 氯化铵和硫酸铵等铵态氮肥与熟石灰混合研磨,都可产生刺激性气味的气体 |
12.下表是固体甲和乙在不同温度时的溶解度,下列说法中正确的是( )
| 温度/℃ | 0 | 20 | 40 | 100 |
| 甲溶解度/克 | 0.173 | 0.165 | 0.121 | 0.076 |
| 乙溶解度/克 | 13.3 | 31.6 | 63.9 | 246 |
| A. | 20℃时物质的溶解能力大小关系:甲大于乙 | |
| B. | 20℃时100克乙物质加入100克水中,所得溶液的质量是200克 | |
| C. | 100℃时乙物质的饱和溶液冷却到室温会析出晶体后,溶液仍为饱和溶液 | |
| D. | 20℃时甲物质的饱和溶液升高温度会变为不饱和溶液 |
19.某化学反应的微观示意图如图所示,根据该图得出的结论,正确的是( )
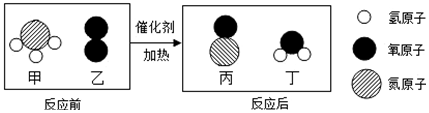

| A. | 四种物质中乙、丙、丁都属于氧化物 | |
| B. | 化学反应前后分子种类没有发生变化 | |
| C. | 丙物质中氮、氧元素的质量比为7:8 | |
| D. | 反应前后只有氮元素的化合价发生了变化 |
9.实验小组用如图的装置进行实验.
请你归纳实验目的:加热氯酸钾和二氧化锰的混合物制取氧气并测量收集氧气的体积.
| 实 验 步 骤 | 简 答 |
(1)称取3g氯酸钾与少量二氧化锰混合后放入装置①的试管中,点燃酒精灯. | 装入药品前要检查装置的气密性 ; 分别用中文名称和化学符号写出a试管中发生反应的表达式:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑. |
(2)加热试管一段时间后,再用橡皮管连接a、b;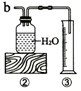 当装置②中水面不再下降,断开a、b,移去酒精灯. | 为什么“加热试管一段时间后,再用橡皮管连接a、b”?原因是:一开始排出的是试管中的空气; ③中使用量筒的作用是通过测量水的体积测量收集的氧气体积. |
16.某物质(仅含一种溶质)的溶液在t℃时,恒温蒸发掉10g水,析出了2g晶体,再恒温蒸发掉10g水,又析出了3g晶体,则下列说法正确的是( )
| A. | 原溶液中t℃时一定是饱和溶液 | |
| B. | t℃时该溶质溶解度为20克 | |
| C. | t℃时该溶质溶解度为30克 | |
| D. | 最后剩余溶液的溶质质量分数比原溶液的溶质质量分数小 |
13.有一包白色固体,可能含有CuCl2、CaCO3、NaOH、Ba(OH)2、BaCl2、Na2SO4中的几种.为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
①取试样溶于水,搅拌、过滤,得到无色澄清溶液A和白色沉淀B;
②取上述无色澄清溶液A,通入适量的CO2,生成白色沉淀C;
③取上述白色沉淀B,加入过量的稀硝酸,沉淀全部消失.
综合上述实验现象,下列判断正确的是( )
| A. | 由①得原白色固体中一定不含CuCl2,一定含量有CaCO3 | |
| B. | 由②③得原白色固体中一定含有Ba(OH)2,一定不含量有Na2SO4 | |
| C. | 由实验现象判断,白色固体中至少有3种固体 | |
| D. | 由实验现象判断,白色固体的组成可有5种情况 |
14. 不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
(1)碳酸钠、碳酸氢钠溶液都能使紫色石蕊试液变成蓝色.
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH增大(填“增大”、“减小”或“不变”),发生反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑.
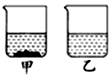
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是Na2CO3(填化学式),加入的质量m的范围为:大于9.6g小于等于21.9g.
 不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示| 温度/℃ | 0 | 20 | 40 | 60 |
| 碳酸钠 | 7.0 | 21.8 | 48.8 | 46.4 |
| 碳酸氢钠 | 6.9 | 9.6 | 12.7 | 16.4 |
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH增大(填“增大”、“减小”或“不变”),发生反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑.
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是Na2CO3(填化学式),加入的质量m的范围为:大于9.6g小于等于21.9g.