题目内容
1.铁锈组分较复杂,某兴趣小组展开了对铁锈成分的研究,某铁锈成分为Fe2O3•xH2O和FeCO3.为确定其组成,兴趣小组称取此铁锈样品25.4g,在科研人员的指导下用图1装置进行实验.
【查阅资料】①Fe2O3•xH2O失去结晶水温度为110℃,FeCO3在282℃分解为FeO和CO2.
②温度高于500℃时铁的氧化物才能被CO还原.
?用CO还原Fe2O3炼铁的过程大致分为三个阶段:
阶段1:3Fe2O3+CO$\frac{\underline{\;500~600℃\;}}{\;}$2Fe3O4+CO2
阶段2:Fe3O4+CO$\frac{\underline{\;600~700℃\;}}{\;}$ 3FeO+CO2
阶段3:FeO+CO $\frac{\underline{\;>700℃\;}}{\;}$ Fe+CO2
(1)装配好实验装置后,首先要检查装置气密性.
(2)装置A中的反应为:H2C2O4(草酸)$→_{△}^{浓硫酸}$CO↑+CO2↑+H2O.通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放c(选填序号).
a.浓硫酸b.澄清的石灰水c.氢氧化钠溶液
(3)现控制D装置中的温度为300℃对铁锈进行热分解,直至D装置中剩余固体质量不再变化为止,冷却后装置E增重3.6g,装置F增重2.2g.则样品中FeCO3的质量m(FeCO3)=5.8g,x=2.
(4)若缺少G装置,测得的m(FeCO3)偏大(选填“偏大”、“偏小”、“不变”,下同),x的值会不变.
(5)将上述300℃热分解后的D装置中剩余固体继续分阶段升温,进行CO还原铁的氧化物炼铁过程的探究.加热时测定D中剩余固体质量随温度变化的曲线如图2所示.图中M点对应的a=18.0.
分析 (1)装配好实验装置后,首先要检查装置气密性;
(2)氢氧化钠溶液能够吸收二氧化碳气体;
(3)控制D装置中的温度为300℃对铁锈进行热分解,D装置中,Fe2O3•xH2O失去结晶水,FeCO3分解为FeO和CO2,冷却后装置E增重3.6g,说明结晶水的质量是3.6g,装置F增重2.2g,说明碳酸亚铁分解生成了2.2g二氧化碳;
(4)G装置能够防止空气中的水蒸气和二氧化碳进入F装置中;
(5)图中M点对应的是氧化亚铁的质量,G点对应的是铁的质量.
解答 解:(1)装配好实验装置后,首先要检查装置气密性.
故填:检查装置气密性.
(2)通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放氢氧化钠溶液,用来吸收反应生成的二氧化碳气体.
故填:c.
(3)冷却后装置E增重3.6g,说明反应生成了3.6g水,装置F增重2.2g,说明反应生成了2.2g二氧化碳,
设碳酸亚铁的质量为m,
FeCO3$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO2↑,
116 44
m 2.2g
$\frac{116}{m}$=$\frac{44}{2.2g}$,
m=5.8g,
则样品中氧化铁质量为:25.4g-3.6g-5.8g=16g,
根据题意有:$\frac{160}{16g}$=$\frac{18x}{3.6g}$,
x=2,
故填:5.8;2.
(4)若缺少G装置,空气中的水蒸气和二氧化碳会进入F装置,导致二氧化碳质量偏大,从而导致测得的m(FeCO3)偏大,空气中的水蒸气不能进入E装置中,因此x的值不变.
故填:偏大;不变.
(5)设氧化亚铁质量为y,
图中M点对应的a是氧化亚铁的质量,G点对应的是铁的质量,铁的质量是14.0g,
根据题意有:y×$\frac{56}{72}$×100%=14.0g,
y=18.0g,
故填:18.0.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 阅读快车系列答案
阅读快车系列答案| A. | 空气 | B. | “温泉”矿泉水 | C. | “漓泉”啤酒 | D. | 浮有冰的水 |
 ”和“
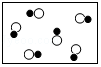
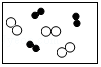
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物质X,微观过程如图所示.下列说法正确的是( )
| A. | 在反应过程中A2和B2分子保持不变 | |
| B. | 该反应为氧化反应 | |
| C. | 参加反应的A2与B2分子数之比为3:1 | |
| D. | 物质X含4种元素 |
| A. | 金刚石用于裁玻璃-------硬度大 | |
| B. | 一氧化碳用于冶炼金属--------氧化性 | |
| C. | 二氧化碳用于灭火------能与水反应 | |
| D. | 活性炭用于净水-------吸附性 |
| A. | 食物腐败 | B. | 海水晒盐 | C. | 玻璃破碎 | D. | 火药爆炸 |

 ”、“
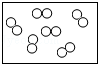
”、“ ”分别表示不同元素的原子,其中表示化合物的是( )
”分别表示不同元素的原子,其中表示化合物的是( )