题目内容
1.实验室中,利用下列装置可以制取某些气体,请回答下列问题.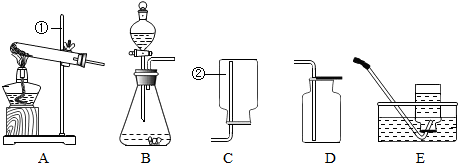
(1)写出带标号的仪器的名称:①铁架台;②集气瓶.
(2)向气体发生装置内加入药品前,应该进行的操作是检查装置气密性.
(3)实验室若用高锰酸钾制取氧气,选择的发生装置是A;反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)若用E装置收集的氧气并完成铁丝在氧气中的燃烧实验,在集气瓶中留一定量的水,目的是防止铁的熔化物溅落而炸裂集气瓶,反应的现象是剧烈燃烧、火星四射、放出热量、生成黑色固体,反应的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(5)乙炔又称电气石,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属,实验室用块状电石(固体)与水反应制取乙炔.你认为制取乙炔应选择的发生装置是B;最佳的收集装置是C或E.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
(4)铁丝在纯氧中燃烧的现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体;还要注意瓶底放少量细沙或少量的水,防止铁的熔化物溅落而炸裂集气瓶.
(5)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置.
解答 解:(1)根据实验室常用仪器可知:a是铁架台;b是集气瓶.
(2)制取气体时都必须检查氢气的气密性,以防装置漏气影响实验结果.
故填:检查装置气密性.
(3)用高锰酸钾制氧气时需要加热,应选用的发生装置是A装置;反应的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用E装置收集;
高锰酸钾受热分解的文字表达式为:
(4)铁和氧气在点燃的条件下生成四氧化三铁,反应的化学方程式是:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;铁丝在纯氧中燃烧的现象是:剧烈燃烧、火星四射、放出热量、生成黑色固体;还要注意瓶底放少量细沙或少量的水,防止铁的熔化物溅落而炸裂集气瓶;故答案为:剧烈燃烧、火星四射、放出热量、生成黑色固体;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;防止铁的熔化物溅落而炸裂集气瓶;
(5)实验室用块状电石(固体)与水反应制取乙炔.不需要加热,应该用B装置作为发生装置;
乙炔又称电气石,是一种无色、无味、密度比空气略小,不溶于水的气体,可以用向下排空气法收集或排水法收集,密度比空气大,可以用向上排空气法收集.
答案:
(1)a铁架台;b集气瓶.
(2)检查装置气密性;
(3)A;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(4)防止铁的熔化物溅落而炸裂集气瓶;剧烈燃烧、火星四射、放出热量、生成黑色固体;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(5)B;C或E.
点评 本题主要考查仪器的用途、文字表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

| 原子种类 | 质子数 | 中子数 | 核外电子数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
| A. | 镁条和盐酸反应会放热 | |
| B. | 铁钉完全浸没在蒸馏水中,一天后观察到大量铁锈 | |
| C. | 黄铜片和铜片相互刻画时,铜片上留下的痕迹更明显 | |
| D. | 向石蕊溶液中通入二氧化碳,溶液变红 |




 A~G为初中化学常见的物质,它们之间的转换关系如图所示(只略去反应①的部分产物).其中A为一种无色液体,B是紫红色金属;D、F为黑色固体.
A~G为初中化学常见的物质,它们之间的转换关系如图所示(只略去反应①的部分产物).其中A为一种无色液体,B是紫红色金属;D、F为黑色固体.
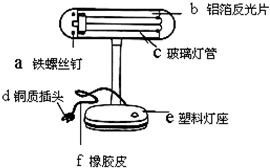 青少年一定要爱护眼睛,在光线不足时看书、写字要用照明工具.如图是一种照明用台灯,请回答下列问题:
青少年一定要爱护眼睛,在光线不足时看书、写字要用照明工具.如图是一种照明用台灯,请回答下列问题: 浑浊的河水可通过静置沉淀、吸附沉淀、过滤等操作来净化.
浑浊的河水可通过静置沉淀、吸附沉淀、过滤等操作来净化.