题目内容
9.下列各组微粒中,属于同一种元素的是( )| A. | Cl和Cl- | B. | Co和CO | C. | H和He | D. | 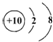 和 和  |
分析 根据元素是具有相同核电荷数(即核内质子数)的同一类原子的总称,进行分析解答本题.
解答 解:A、Cl和Cl-的核电荷数都是17,不同的是Cl核外有17个电子,而Cl-核外有18个电子,但是它们具有相同的核电荷数,同属于氯元素;故A正确;
B、Co是钴的元素符号,CO是一氧化碳,不是一种元素;故B错误;
C、H和He的原子内质子数不同,所以是两种不同的元素,故C错误;
D、两种微粒的质子数(核电荷数)不同,不属于同一种元素.故D错误.
故选A.
点评 本题考查学生对元素的概念的理解与掌握,并应用才知识进行分析解题的能力.

练习册系列答案
相关题目
18. 小丽喜食豆腐,今天,小丽让妈妈为她做菠菜炒豆腐,可小丽的妈妈却告诉她菠菜不能与豆腐同食.
小丽喜食豆腐,今天,小丽让妈妈为她做菠菜炒豆腐,可小丽的妈妈却告诉她菠菜不能与豆腐同食.
【提出问题】菠菜为什么不能与豆腐同食?
【查阅资料】草酸钙(CaC2O4)是不能被人体吸收的沉积物.豆腐中含有较多的钙盐 如硫酸钙(CaSO4)等,菠菜、洋葱、竹笋中含有丰富的草酸(H2C2O4)、草酸钠(Na2C2O4),豆腐和上述几种蔬菜混合食用,可能诱发“结石”症.
(1)由草酸的化学式可知草酸由C、H、O三种元素组成.
(2)草酸与硫酸钙反应的化学方程式为H2C2O4+CaSO4?CaC2O4↓+H2SO4,请写出草酸钠与硫酸钙反应的化学方程式:Na2C2O4+CaSO4═Na2SO4+CaC2O4↓.
【提出猜想】菠菜与豆腐同食可能会诱发“结石”症.
【设计实验】
【发现新问题】被溶解的沉淀是什么?产生的气体又是什么?于是她又设计如下实验进一步探究:
已知草酸分解的化学方程式为:H2C2O4$\stackrel{187℃}{→}$H2O+CO2↑+CO↑
利用图Ⅱ①和图Ⅱ②加热草酸晶体,以验证草酸受热是否分解.连续加热一段时间后的现象是:图Ⅱ①:试管里澄清石灰水先变浑浊,后又变澄清,其原因CaCO3+H2O+CO2═Ca(HCO3)2;图Ⅱ②:试管里澄灰水只变浑浊其原因是草酸气体与石灰水反应生成草酸钙;能验证草酸受热分解的装置是1(填图Ⅱ中的编号“①”或“②”),理由是:因为①中有冷却装置(从装置的特点分析).
 小丽喜食豆腐,今天,小丽让妈妈为她做菠菜炒豆腐,可小丽的妈妈却告诉她菠菜不能与豆腐同食.
小丽喜食豆腐,今天,小丽让妈妈为她做菠菜炒豆腐,可小丽的妈妈却告诉她菠菜不能与豆腐同食.【提出问题】菠菜为什么不能与豆腐同食?
【查阅资料】草酸钙(CaC2O4)是不能被人体吸收的沉积物.豆腐中含有较多的钙盐 如硫酸钙(CaSO4)等,菠菜、洋葱、竹笋中含有丰富的草酸(H2C2O4)、草酸钠(Na2C2O4),豆腐和上述几种蔬菜混合食用,可能诱发“结石”症.
(1)由草酸的化学式可知草酸由C、H、O三种元素组成.
(2)草酸与硫酸钙反应的化学方程式为H2C2O4+CaSO4?CaC2O4↓+H2SO4,请写出草酸钠与硫酸钙反应的化学方程式:Na2C2O4+CaSO4═Na2SO4+CaC2O4↓.
【提出猜想】菠菜与豆腐同食可能会诱发“结石”症.
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①将菠菜在少量开水中煮沸2min~3min,取1mL~2mL滤液于试管中,丙滴加少量CaSO4或CaCl2溶液 | 产生白色沉淀 | 有草酸钙生成 |
| ②在步骤①的沉淀物中加入过量稀盐酸 | 沉淀部分溶解且产生气泡 | 被溶解的沉淀一定不是CaC2O4 |
| 实验步骤 | 实验现象 | 实验结论 |
| ③将步骤②产生的气体通入澄清的石灰水中 | 澄清的石灰水变浑浊 | 产生的气体是CO2步骤②被溶解的沉淀是碳酸钙 |
利用图Ⅱ①和图Ⅱ②加热草酸晶体,以验证草酸受热是否分解.连续加热一段时间后的现象是:图Ⅱ①:试管里澄清石灰水先变浑浊,后又变澄清,其原因CaCO3+H2O+CO2═Ca(HCO3)2;图Ⅱ②:试管里澄灰水只变浑浊其原因是草酸气体与石灰水反应生成草酸钙;能验证草酸受热分解的装置是1(填图Ⅱ中的编号“①”或“②”),理由是:因为①中有冷却装置(从装置的特点分析).


 乙醇汽油作为一种新型清洁燃料,符合我国能源替代战略和可再生能源发展方向,技术上成熟安全可靠,在我国完全适用,具有较好的经济效益和社会效益,请回答以下有关的问题
乙醇汽油作为一种新型清洁燃料,符合我国能源替代战略和可再生能源发展方向,技术上成熟安全可靠,在我国完全适用,具有较好的经济效益和社会效益,请回答以下有关的问题