题目内容
10. 某化学活动小组用稀盐酸对方镁石中MgO含量进行测定(杂质不与盐酸反应且不溶于水),实验后得到一无色残液.为防止直接排放造成环境污染,对其组成进一步进行探究.
某化学活动小组用稀盐酸对方镁石中MgO含量进行测定(杂质不与盐酸反应且不溶于水),实验后得到一无色残液.为防止直接排放造成环境污染,对其组成进一步进行探究.【活动一】过滤该残液,取100g滤液,向其中不断加入5%的氢氧化钠溶液,所得实验数据如下表:
| 氢氧化钠溶液的质量/g | 4 | 8 | 12 | 16 | 28 | 32 |
| 生成沉淀的质量/g | 0 | 0 | 0.145 | 0.29 | 0.58 | 0.58 |
(2)选择合理的数据,计算100g滤液中溶质的质量分数(若有多种溶质,任选一种,列出计算过程).
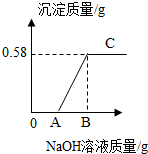
【活动二】小组同学将测得沉淀质量与所加入氢氧化钠溶液质量绘成坐标图如右.
(3)A点时,溶液中溶质的化学式为NaCl、MgCl2;C点时溶液的pH值>7(填“>”、“=”或“<”).
(4)根据活动一的实验数据分析,A、B点的数值分别为8、24.
分析 氧化镁和稀盐酸反应生成氯化镁和水,氯化镁和氢氧化钠反应生成白色沉淀氢氧化镁和氯化钠,根据提供的数据和反应的化学方程式可以进行相关方面的判断和计算.
解答 解:(1)加入氢氧化钠溶液时,开始不产生沉淀,说明溶液中含有稀盐酸,因此该滤液中含有的溶质是过量的氯化氢和反应生成的氯化镁,
故填:HCl、MgCl2.
(2))设:100g废水中氯化镁的质量为x,
MgCl2+2NaOH═Mg(OH)2↓+2NaCl,
95 58
x 0.58g
$\frac{95}{x}$=$\frac{58}{0.58g}$,
x=0.95g,
100g滤液中氯化镁的质量分数为:$\frac{0.95g}{100g}$×100%=0.95%,
答:100g滤液中氯化镁的质量分数为0.95%.
(3)A点时,溶液中溶质有反应生成的氯化钠和没有反应的氯化镁;
C点时氢氧化钠过量,溶液显碱性,pH值大于7.
故填:NaCl、MgCl2;>.
(4)由表中数据和图中信息可知,从8g到12g增加4g氢氧化钠溶液所产生的沉淀,和由12g到16
g增加4g氢氧化钠溶液所产生的沉淀质量相等,所以可以下结论8g时盐酸已经完全反应.氢氧化钠恰好和稀盐酸完全反应时消耗氢氧化钠溶液的质量是8g,因此A点的值是8;
由表中数据和图中信息可知,加入4g氢氧化钠溶液时产生的沉淀质量是0.145g,因此产生0.58g沉淀时消耗氢氧化钠溶液质量应该是16g,因此B点的值是:16+8=24,
故填:8;24.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
15.小玲同学对所学的部分化学知识归纳如下,其中不完全正确的是( )
| A.化学材料 | B.食品安全 |
| ①毛织品和棉织品的区别-燃烧后闻气味 ②钢筋混凝土、汽车轮胎-复合材料 ③玻璃、陶瓷、水泥-无机非金属材料 | ①工业酒精-含有甲醇等物质,不能饮用 ②含有塑化剂的食物、饮料不能食用 ③黄曲霉素-属于有机物,霉变食物不能食用,会诱发癌症 |
| C.用化学“眼观”分析 | D.低碳经济 |
| ①区别食醋和酒精-闻气味 ②氧气可以支持燃烧,说明氧气具有可燃性 ③用水灭火是降低可燃物的着火点 | ①改造或淘汰高耗能、高污染产业 ②开发新能源代替传统能源 ③减少使用一次性筷子 |
| A. | A | B. | B | C. | C | D. | D |
2.某固体样品可能由硝酸钠、硝酸钡、硫酸铜、碳酸钾、碳酸钠中的一种或几种组成.为探究其组成,取固体样品13g加足量的水溶解得无色溶液,再加入过量的氯化钙溶液,得到干燥沉淀10g.下列判断正确的是( )
| A. | 该固体样品中一定含有碳酸钾 | |
| B. | 该固体样品中一定含有碳酸钠和硝酸钠 | |
| C. | 该固体样品中可能含有硝酸钠和硝酸钡 | |
| D. | 加足量的水溶解得无色溶液,说明样品中一定没有硫酸铜 |
20.下列关于“生活中的化学”的叙述中,不正确的是( )
| A. | 干冰可用于人工降雨 | |
| B. | 甲醛水溶液可用于海产品保鲜 | |
| C. | 食用加碘食盐可预防甲状腺肿大 | |
| D. | 净水方法中,净化程度最高的是蒸馏 |