题目内容
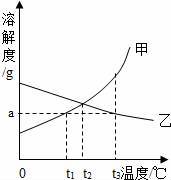
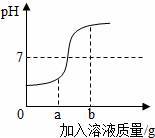
在用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.
(1)该反应的化学方程式为: .
(2)该实验操作是将 滴加到另一种溶液中.
(3)当加入溶液的质量为ag时,所得溶液中的溶质为(写化学式) .
(4)当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈 色.

【考点】溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
【专题】压轴实验题;物质的变化与性质;化学反应的基本类型和能量变化;溶液、浊液与溶解度;常见的酸 酸的通性;常见的碱 碱的通性.
【分析】(1)氢氧化钠和盐酸反应能生成氯化钠和水;
(2)盐酸显酸性,pH小于7,氢氧化钠溶液显碱性,pH大于7;
(3)当盐酸过量时,盐酸和氢氧化钠反应后的溶液中含有氯化氢、氯化钠;
(4)显碱性的溶液能使酚酞试液变红色.
【解答】解:(1)稀盐酸和氢氧化钠溶液反应的化学方程式为:NaOH+HCl=NaCl+H2O.
(2)开始时溶液的pH小于7,说明是把氢氧化钠溶液滴加到稀盐酸中.故填:氢氧化钠溶液.
(3)当加入溶液的质量为ag时,溶液的pH小于7,说明盐酸过量,所得溶液中的溶质为氯化氢和氯化钠.故填:HCl、NaCl.
(4)当加入溶液的质量为bg时,溶液的pH大于7,溶液显碱性,显碱性的溶液能使酚酞试液变红色.故填:红.
【点评】本题主要考查溶液的酸碱性和pH之间的关系,同时考查了化学方程式的书写方面的知识,书写化学方程式时要注意遵循质量守恒定律.

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案