题目内容
15.(1)氢气在氯气(Cl2)中燃烧生成氯化氢气体(H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl).如果燃烧0.4g氢气可以得到氯化氢气体的质量是多少?(2)若将上述所得氯化氢气体通入85.4g水中完全溶解形成盐酸,求该盐酸的溶质质量分数.
分析 (1)根据化学方程式中氢气的质量可求生成的氯化氢质量;
(2)根据溶质质量分数公式计算.
解答 解:(1)设生成氯化氢气体的质量为x.
H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl
2 73
0.4g x
$\frac{2}{0.4g}$=$\frac{73}{x}$
x=14.6g
答:生成氯化氢气体的质量为14.6g
(2)该盐酸的溶质质量分数为$\frac{14.6g}{14.6g+85.4g}$×100%=14.6%
答:盐酸的溶质质量分数为14.6%.
点评 此题是对化学基本计算的考查,解题的关键是对有关溶质质量分数和化学方程式基本计算的掌握,属基础性知识考查题.

练习册系列答案
相关题目
17.下列物品所使用的主要材料属于有机合成材料的是( )
| A. | 陶瓷茶杯 | B. | 塑料凉鞋 | C. | 纯棉T恤 | D. | 不锈钢饭盒 |
18.下列物质属于化合物的是( )
| A. | 河水 | B. | 大理石 | C. | 氮气 | D. | 二氧化硫 |
3.由燃烧的条件判断下列说法正确的是( )
| A. | 燃烧一定会引起爆炸 | |
| B. | 只要外界条件足够,所有物质都能燃烧 | |
| C. | 用玻璃杯罩住点燃的蜡烛,火焰熄灭是因为隔绝了空气 | |
| D. | 水能灭火主要是因为水蒸发吸热,降低了可燃物的着火点 |
20.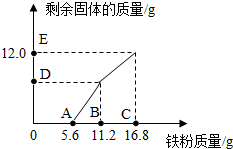 往200g FeCl3和CuCl2的混合溶液中加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe=3FeCl2 CuCl2+Fe=FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
往200g FeCl3和CuCl2的混合溶液中加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe=3FeCl2 CuCl2+Fe=FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
 往200g FeCl3和CuCl2的混合溶液中加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe=3FeCl2 CuCl2+Fe=FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
往200g FeCl3和CuCl2的混合溶液中加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe=3FeCl2 CuCl2+Fe=FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )| A. | B点后溶液的颜色为蓝色 | |
| B. | D点对应纵坐标为6.4 | |
| C. | 该200g溶液中的CuCl2 质量分数为6.75% | |
| D. | 取DE两点间的剩余固体加入盐酸,均有气泡产生 |