题目内容
今年我国“世界环境日”的主题是向污染宣战,某化工厂排放的废水中含有氢氧化钾和碳酸钾.提取50g废水样品于集气瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,共得到硫酸钾98g,同时收集到2.2g二氧化碳,求该废水样品中氢氧化钾的质量.
| 根据化学反应方程式的计算. . | |
| 专题: | 有关化学方程式的计算. |
| 分析: | 先利用质量守恒定律计算出反应消耗的稀硫酸的质量,再根据二氧化碳的质量结合化学方程式计算出废水中碳酸钾消耗的硫酸溶液的质量,利用质量差即可计算出氢氧化钾消耗的硫酸质量,根据硫酸与氢氧化钾反应的化学方程式即可解答. |
| 解答: | 解:反应消耗的硫酸质量为:98g+2.2g﹣50g=50.2g 设,碳酸钾消耗的硫酸溶液质量为x, K2CO3+H2SO4=K2SO4+H2O+CO2↑; 98 44 x•10% 2.2g
x=49g 故氢氧化钾消耗的硫酸溶液质量为:50.2g﹣49g=3.2g 设,废水样品中氢氧化钾的质量为y, 2KOH+H2SO4=K2SO4+ 112 98 y 3.2g×10%
y=0.366g 答:废水样品中氢氧化钾的质量是0.366g; |
| 点评: | 解答本题的关键是利用质量守恒定律计算出消耗硫酸溶液质量,在利用化学方程式计算即可. |

 阅读快车系列答案
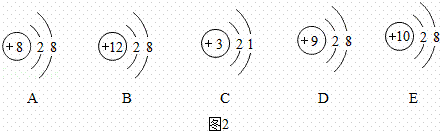
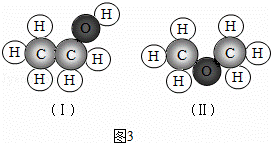
阅读快车系列答案两种化合物都有甜味,下列推测正确的是( )
|
| A. | 组成元素一定相同 |
|
| B. | 构成分子的原子个数一定相同 |
|
| C. | 分子中某些原子的结合方式可能是相似的 |
|
| D. | 性质、组成和结构完全相同 |
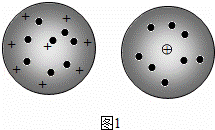
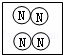
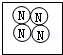
如图中能表示2N2的是( )
|
| A. |
| B. |
| C. |
| D. |
|
人体一些液体的正常pH范围如下,其中酸性最强的是( )
|
| A. | 胃液0.9~1.5 | B. | 胆汁7.1~7.3 | C. | 血浆7.35~7.45 | D. | 尿液4.7~8.4 |
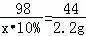
 2H2O
2H2O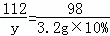



 2S2O3
2S2O3