题目内容
14. 现有17.1%的Al2(SO4)3溶液,请按要求回答:
现有17.1%的Al2(SO4)3溶液,请按要求回答:(1)200g上述溶液中所含溶质的质量为34.2g.
(2)已知:向Al2(SO4)3溶液 中加入NaOH溶液时,反应分两步进行:第一步反应为
Al2(SO4)3+6NaOH═2Al(OH)3↓+3Na2SO4,第二步反应为Al(OH)3+NaOH═NaAlO2(偏铝酸钠)+2H2O.偏铝酸钠易溶于水.则200g上述溶液与10%的氢氧化钠溶液反应,生成沉淀的质量最大时,消耗NaOH溶液的质量为多少?(请写出计算过程)
(3)向上述溶液中逐滴加入10%的氢氧化钠溶液并不断搅拌.请在如图中画出沉淀质量的变化曲线.
(4)另取17.1%的Al2(SO4)3溶液边搅拌边加入10%的氢氧化钠溶液,有关反应物与生成物的质量如表:
| 物质 | Al2(SO4)3 | NaOH | Na2SO4 | X | Al(OH)3 | H2O |
| 质量/g | 34.2 | 28.0 | 42.6 | 8.2 | a | 3.6 |
分析 根据已有的溶液的计算方法进行分析解答,根据题干提供的条件结合化学方程式计算即可,根据反应物和生成物书写反应的化学方程式.
解答 解:(1)200g17.1%的溶液中含有溶质的质量为:200g×17.1%=34.2g,故填:34.2;
(2)解:设生成沉淀质量最大时消耗氢氧化钠溶液的质量为x,生成氢氧化铝的质量为y
Al2(SO4)3+6NaOH=2Al(OH)3↓+3Na2SO4
342 240 156
34.2g x×10% y
$\frac{342}{34.2g}=\frac{240}{x×10%}$
解得 x=240g
$\frac{342}{34.2g}=\frac{156}{y}$
y=15.6g
答:生成沉淀质量最大时消耗氢氧化钠溶液的质量为240g
(3)设生成的氢氧化铝完全溶解需要氢氧化钠溶液的质量为z,则有:
Al(OH)3+NaOH═NaAlO2+2H2O
78 40
15.6g z×10%
$\frac{78}{15.6g}=\frac{40}{z×10%}$
z=80g
故可以画出图象为: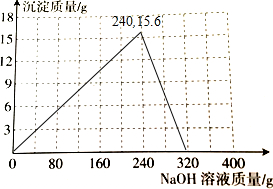
(4)根据质量守恒定律,氢氧化铝的质量为:34.2g+28g-42.6g-8.2g-3.6g=7.8g,硫酸铝能与氢氧化钠反应生成氢氧化铝、偏铝酸钠、硫酸钠和水,故填:7.8; Al2(SO4)3+7NaOH=2Al(OH)3↓+3Na2SO4+NaAlO2+2H2O.
点评 本题考查的是根据化学方程式的计算的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
2.化学与生活密切相关,生活中的下列做法不合理的是( )
| A. | 高楼发生火灾,乘电梯逃生 | |
| B. | 用白醋除水壶中的水垢 | |
| C. | 家用电器着火,应先切断电源再用干粉灭火器灭火 | |
| D. | 洒在实验桌上的少量酒精着火,迅速用湿布盖灭 |
6.下列实验操作中,不正确的是( )
| A. |  点燃酒精灯 | B. | 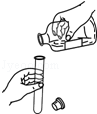 倾倒液体 | C. | 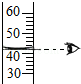 液体的量取 | D. | 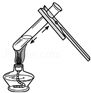 给液体加热 |
3.下列说法正确的是( )
| A. | 纯碱不是碱 | B. | 盐酸不是混合物 | C. | 苛性钠不是碱 | D. | 消石灰不是碱 |
4.据央视《每周质量报告》的3•15节目《“健美猪”真相》的报道,河南孟州等地养猪场采用违禁动物药品“瘦肉精”饲养,有毒猪肉部分流向河南双汇集团下属分公司济源双汇食品有限公司.“瘦肉精”的主要成分为盐酸克伦特罗(Clenbuterol).下列不属于盐酸克伦特罗物理性质的是( )
| A. | 熔点为174~175.5℃ | |
| B. | 无色微结晶粉末,无臭,味微苦 | |
| C. | 加热到172℃时才能分解 | |
| D. | 易溶于水、甲醇、乙醇,微溶于氯仿,不溶于苯 |
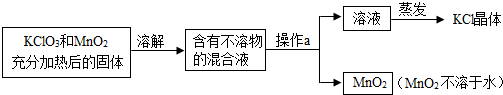
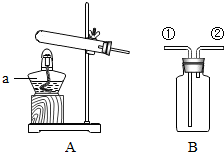 某学校实验小组的同学欲用氯酸钾来制取氧气,并回收提纯氯化钾和二氧化锰.
某学校实验小组的同学欲用氯酸钾来制取氧气,并回收提纯氯化钾和二氧化锰.