题目内容
6.某化合物一个分子X2O中电子数为10,则X的核电荷数为( )| A. | 1 | B. | 2 | C. | 8 | D. | 5 |
分析 根据原子中,核电荷数=电子数进行计算.
解答 解:某化合物一个分子X2O中电子数为10,则一个X原子中电子数为(10-8)÷2=1,根据核电荷数=电子数可知,则X的核电荷数为1.
故选:A.
点评 本题考查学生对在原子中,核电荷数=电子数的牢记与掌握,并能应用于解题.

练习册系列答案
相关题目
17.某同学取一块表面完全锈蚀的生铁片进行了以下探究:
(1)实验:
(2)表达:步骤②的化学方程式为Fe+2HCl═FeCl2+H2↑、Fe2O3+6HCl═2FeCl3+3H2O.
(3)拓展:取2枚未生锈的铁钉,一枚部分浸入蒸馏水、另一枚部分浸入盐水,生锈较快的是部分浸入食盐水的铁钉.
(1)实验:
| 步骤 | 操作 | 现象 | 结论 |
| ① | 取适量固体于试管中加热,用一干冷的玻片置于试管口上方. | 玻片上有水雾 | 固体中含有水. |
| ② | 取适量固体于试管中,加入足量的稀盐酸,观察溶液颜色. | 溶液呈黄色. | 固体中含有Fe2O3. |
| ③ | 收集步骤②试管中产生的气体, 点燃. | 有爆鸣声. | 固体中含有 铁. |
| ④ | 将上面反应后的混合液过滤. | 有黑色固体. | 黑色固体的主要成分是炭. |
(3)拓展:取2枚未生锈的铁钉,一枚部分浸入蒸馏水、另一枚部分浸入盐水,生锈较快的是部分浸入食盐水的铁钉.
14.下列生活中的说法不正确的是( )
| A. | 尽量避免钢铁制品与氧气、水、盐或酸性物质接触 | |
| B. | 空气中含量最多的气体是氮气 | |
| C. | 用喷漆的方法防止自行车链条锈蚀 | |
| D. | 铁丝表面的锈应及时去掉 |
1.盛放油罐车内的石油产品,震荡时可以产生静电而引起火灾,所以油罐车尾部有一条拖地的铁链,这里利用铁的( )
| A. | 延展性 | B. | 导电性 | C. | 硬度小 | D. | 熔点高 |
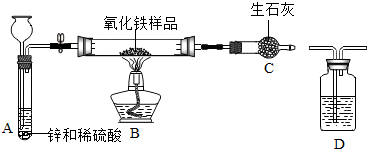
11.某小组的同学用如图所示装置对氧化铁粉末(含少量铁粉)样品进行实验,图中铁架台等装置已略去.请回答:
(1)小组同学在实验操作时,应注意加热前先通一会儿氢气,目的是排尽空气,防止加热时发生爆炸.
(2)请完成表格.(H2的化学性质与CO相似):
(3)数据记录和处理:经规范的操作和正确称量,得到如下两组数据(B中反应完全,C中吸收完全):
通过计算发现,用得到的两组数据求出的样品中氧化铁的质量分数不同.你觉得应选①组数据,样品中氧化铁的质量分数是80%.
(4)问题和讨论:经讨论,同学们对装置进行了改进,在AB(填2个装置代号)之间增加了如图所示的D装置,再次实验后,用得到的两组数据求出的样品中氧化铁的质量分数基本相同.
图D装置里的液体是浓硫酸.

(1)小组同学在实验操作时,应注意加热前先通一会儿氢气,目的是排尽空气,防止加热时发生爆炸.
(2)请完成表格.(H2的化学性质与CO相似):
| 实验现象 | 化学方程式 |
| A中反应产生大量气泡; | A中:Zn+H2SO4═ZnSO4+H2↑. |
| B中红色粉末逐渐变黑色; | B中:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2. |
| 反应前 | 氧化铁完全反应后 | |
| ①组 | B:玻璃管质量32.4g,氧化铁样品的质量10.0g | B:玻璃管和管内固体物质的质量40.0g |
| ②组 | C:干燥管和生石灰质量40.Og | C:干燥管和管内固体物质的质量43.0g |
(4)问题和讨论:经讨论,同学们对装置进行了改进,在AB(填2个装置代号)之间增加了如图所示的D装置,再次实验后,用得到的两组数据求出的样品中氧化铁的质量分数基本相同.
图D装置里的液体是浓硫酸.
18.下列做法不会导致中毒的是( )
| A. | 用氯化钠配制生理盐水 | B. | 用工业用盐亚硝酸钠烹调食物 | ||
| C. | 用工业酒精配制白酒 | D. | 用胆矾对饮用井水消毒、杀菌 |
16.下列实验操作,不能达到预期目的是( )
| A. | 用排水集气法可得到比较纯净的氧气 | |
| B. | 用托盘天平称取5.6 g氧化铜粉末 | |
| C. | 用5mL水和5mL酒精配制成10 mL酒精溶液 | |
| D. | 用10 mL量筒量取8.2 mL水 |