题目内容
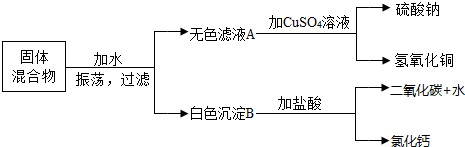
15.有一包白色粉末,可能由:氯化钙、碳酸钠、氯化铜和氢氧化钠中的一种或几种物质组成.为了鉴定其成分,实验如下:(1)将粉末放入足量水中,搅拌,得无色溶液;
(2)在(1)向所得溶液中加入足量的稀盐酸,有气泡冒出.
结论:该白色粉末中一定含有碳酸钠,一定不含有氯化钙、氯化铜;
写出实验(2)中一定发生的反应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑.
分析 根据“白色粉末,可能由:氯化钙、碳酸钠、氯化铜和氢氧化钠中的一种或几种物质组成”,“将粉末放入足量水中,搅拌,得无色溶液”,则一定无氯化铜,根据“在(1)向所得溶液中加入足量的稀盐酸,有气泡冒出”,则推测一定有碳酸钠;既然有碳酸钠,则一定无氯化钙;可能含有氢氧化钠.
解答 解:
根据“白色粉末,可能由:氯化钙、碳酸钠、氯化铜和氢氧化钠中的一种或几种物质组成”,“将粉末放入足量水中,搅拌,得无色溶液”,则一定无氯化铜,根据“在(1)向所得溶液中加入足量的稀盐酸,有气泡冒出”,则推测一定有碳酸钠;既然有碳酸钠,则一定无氯化钙;可能含有氢氧化钠.
碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故答案为:
碳酸钠,氯化钙、氯化铜; Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评 本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.

练习册系列答案
相关题目
10.石油被人们称为“工业的血液”,它没有固定的沸点,通过加热气化、冷凝、分离可得到汽油、煤油等产品,由此可以判定石油属于( )
| A. | 纯净物 | B. | 混合物 | C. | 单质 | D. | 化合物 |
11.化学实验既要操作规范,更要保障安全.下列实验基本操作不符合这一要求的是( )
| A. | 不能直接把鼻孔凑到试剂瓶口闻浓盐酸的气味 | |
| B. | 给试管里的液体加热时,试管口不能对着自己或他人 | |
| C. | 不慎将浓硫酸洒在皮肤上,先用大量水冲,再涂抹氢氧化钠溶液 | |
| D. | 用一氧化碳与氧化铁反应时,先要通入气体将装置内的空气排净后再加热 |
3.下列变化属于化学变化的是( )
| A. | 灯泡通电时发热发光 | B. | 气球爆炸 | ||
| C. | 铁器生锈 | D. | 湿衣服晒干 |