题目内容
把干燥、纯净的氯酸钾和二氧化锰的混合物15.5g装入大试管中,加热制取氧气.待反应完全后,将试管冷却、称量,得到10.7g固体物质.计算制得氧气多少克?混合物中参加反应的氯酸钾质量为多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;
反应前后的固体质量差即为生成氧气的质量;
根据氧气的质量可以计算氯酸钾的质量.
反应前后的固体质量差即为生成氧气的质量;
根据氧气的质量可以计算氯酸钾的质量.
解答:解:
(1)生成氧气的质量为:15.5g-10.7g=4.8g,
(2)设氯酸钾的质量为x
2KClO3
2KCl+3O2↑
245 96
x 4.8g
=
x=12.25g
答案:制得氧气4.8克,参加反应的氯酸钾质量为12.25克.
(1)生成氧气的质量为:15.5g-10.7g=4.8g,
(2)设氯酸钾的质量为x
2KClO3
| ||
| △ |
245 96
x 4.8g
| 245 |
| x |
| 96 |
| 4.8g |
x=12.25g
答案:制得氧气4.8克,参加反应的氯酸钾质量为12.25克.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
氧化铜中混有少量炭粉,提纯的依据或采取的方法是( )
| A、把混合物隔绝空气强热 |
| B、在氧气流中加热混合物 |
| C、氧化铜可溶于水,炭粉不溶 |
| D、在氢气流中加热混合物 |
可用于实验室制取氧气的药品是( )
| A、空气 | B、过氧化氢和二氧化锰 |
| C、二氧化碳 | D、二氧化锰 |
下列实验操作或仪器使用正确的是( )
A、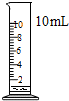 量9.5mL液体 |
B、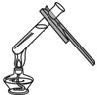 液体加热 |
C、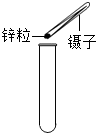 |
D、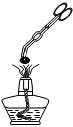 高温煅烧固体 |