题目内容
19.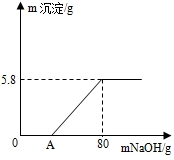 向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答下列问题:
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答下列问题:(1)写出OA段的化学方程式:H2SO4+2NaOH=Na2SO4+2H2O.
(2)加入镁粉的质量为2.4g.
(3)恰好完全反应时,求溶液中溶质的质量分数.
分析 (1)根据开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水进行解答;
(2)根据生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量进行解答;
(3)根据稀硫酸和镁生成硫酸镁和氢气,硫酸镁、稀硫酸和氢氧化钠都会生成硫酸钠,实质是氢氧化钠和硫酸反应生成了硫酸钠进行解答.
解答 解:(1)开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水,化学方程式为:H2SO4+2NaOH=Na2SO4+2H2O;
(2)生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量,由图可知生成氢氧化镁的质量为5.8g,所以加入镁粉的质量=$\frac{24}{24+(16+1)×2}$×100%×5.8g=2.4g;
(3)设生成的硫酸钠是x,
2NaOH----Na2SO4
80 142
80g×20% x
$\frac{80}{80g×20%}$=$\frac{142}{x}$
x=28.4g
所以溶液中溶质的质量分数为:$\frac{28.4g}{100g+80g+2.4g-0.2g-5.8g}$×100%=16.1%.
故答案为:(1)H2SO4+2NaOH=Na2SO4+2H2O;
(2)2.4;
(3)溶液中溶质的质量分数为16.1%.
点评 本题主要考查学生利用化学方程式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
9.下列说法或做法不合理的是( )
| A. | 生病时用药越多越有助康复 | B. | 暖水瓶中薄层水垢用食醋除去 | ||
| C. | 油锅着火时应立即盖上锅盖 | D. | 冰箱中的异味可用活性炭除去 |
10.下列各组物质按照单质、氧化物、混合物的顺序排列的是( )
| A. | 石墨、生石灰、酒精 | B. | 稀有气体、二氧化硫、稀硫酸 | ||
| C. | 氧气、冰水共存物、大理石 | D. | 生铁、水、石油 |
11.如表是氯化钠、氯化铵两种固体在不同温度下的溶解度.
(1)20℃时,氯化铵的溶解度是37.2g
(2)0℃时,氯化钠的饱和溶液与氯化铵的饱和溶液,其溶液中溶质的质量分数:氯化钠>氯化铵(填“>”“=”或“<”).
(3)40℃时,向两只分别盛有40gNaCl和40gNH4Cl固体的烧杯中,各加入100g水,充分溶解后升温至80℃,能形成饱和溶液的溶质是NaCl(填化学式),此时该溶液中溶质与溶剂的质量比为38:100(整数比).
(4)将上述(3)中的不饱和溶液变成饱和溶液,可采用降温方法.
| 温度/ | 0 | 20 | 40 | 60 | 80 | |
| 物质的溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| 氯化铵 | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(2)0℃时,氯化钠的饱和溶液与氯化铵的饱和溶液,其溶液中溶质的质量分数:氯化钠>氯化铵(填“>”“=”或“<”).
(3)40℃时,向两只分别盛有40gNaCl和40gNH4Cl固体的烧杯中,各加入100g水,充分溶解后升温至80℃,能形成饱和溶液的溶质是NaCl(填化学式),此时该溶液中溶质与溶剂的质量比为38:100(整数比).
(4)将上述(3)中的不饱和溶液变成饱和溶液,可采用降温方法.
8.自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用如图表示,下列有关说法错误的是( )
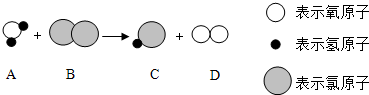

| A. | 反应的基本反应类型是置换反应 | |
| B. | C和D两种粒子的个数比是2:1 | |
| C. | 有的分子由同种原子构成,有的分子由不同种的原子构成 | |
| D. | 在反应中A和D两种物质的质量比是9:8 |
9.下列化学方程式书写正确的是( )
| A. | 铁丝在氧气中燃烧:Fe+O2$\frac{\underline{\;点燃\;}}{\;}$FeO2 | |
| B. | 电解水:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| C. | 铁加入硫酸锌溶液中:Fe+ZnSO4═FeSO4+Zn | |
| D. | 碳酸钠与稀盐酸反应:Na2CO3+2HCl═2NaCl+CO2+H2O |