题目内容
用木炭还原氧化铜的实验如图。
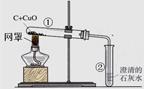
(1)酒精灯加灯罩的目的 ;
(2)刚开始预热,试管②中立即产生气泡,但石灰水不变浑浊,原因是 ;
(3)继续加热,观察到石灰水逐渐变浑浊,黑色粉末中出现红色物质。请你写出带点部分的化学方程式: 、 ;
(4)停止加热时,应先将导管从试管②中撤出,并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出。这样操作的原因是 。
(1)使火焰集中的并提高温度(2)开始排出的是试管内的空气
(3)C+2CuO 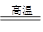 2Cu+CO2↑ CO2+Ca(OH)2==CaCO3
↓+H2O
2Cu+CO2↑ CO2+Ca(OH)2==CaCO3
↓+H2O
(4)防止外面的空气进入玻璃管使铜重新被氧化
【解析】
试题分析:(1)根据酒精灯的使用进行分析,酒精灯加灯罩可以集中火焰,提高温度;
(2)由于试管内有空气,加热时空气体积膨胀,故先出来的气体是空气,空气中的二氧化碳较少,故石灰水不变浑浊;
(3)木碳在高温下还原氧化铜,有红色的铜和二氧化碳生成,则反应的化学方程式为C+2CuO 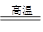 2Cu+CO2↑;生成的二氧化碳与澄清石灰水反应,生成碳酸钙沉淀和水,故能使澄清石灰水变浑浊,则反应的化学方程式为CO2+Ca(OH)2=CaCO3
↓+H2O;
2Cu+CO2↑;生成的二氧化碳与澄清石灰水反应,生成碳酸钙沉淀和水,故能使澄清石灰水变浑浊,则反应的化学方程式为CO2+Ca(OH)2=CaCO3
↓+H2O;
(4)停止加热时,先将导管从试管②中撤出,可防止试管②中的石灰水倒吸入热的试管,使试管炸裂; 用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出,可防止空气进入试管①,而使试管①中生成的灼热的铜再次被氧化。
考点:碳、一氧化碳、氢气还原氧化铜实验
点评:本题主要考查了碳还原氧化铜的实验现象和实验操作,解答这类题目,就要熟记和理解碳还原氧化铜实验的化学反应方程式、操作及注意事项和现象,以及二氧化碳的检验等相关知识,只有这样才能对相关方面的问题做出正确的解答。

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案
某化学兴趣小组按照图1所示装置进行木炭还原氧化铜的实验,很快发现试管①、试管②中分别出现________________的现象.从而得到的结论是________(用化学
方程式表示).在对该实验进行总结时,大家对木炭还原氧化铜的最终产物产生的兴趣:碳还原氧化铜得到氧会不会生成CO?而CuO失去氧会不会生成Cu2O(氧化亚铜)?并为此进行了以下探究过程.
【查阅资料】
①红色固体不仅只有Cu,还有Cu2O
②Cu2O+H2SO4(稀)=Cu+CuSO4+H2O (CuSO4溶于水溶液呈蓝色)
③微量的CO气体能使湿润的黄色氯化钯试纸变蓝色.
【猜想】
(a)红色固体只有Cu,气体只有CO2.
(b)红色固体是________,气体是________.
(c)红色固体是Cu和Cu2O的混合物,气体是CO2和CO的混合物
【探究步骤】
Ⅰ.兴趣小组首先对C和CuO反应的气体产物进行了探究.如图2所示是他们进行实验的部分流程(装置气密性良好,浓硫酸起干燥作用)通过以上实验,观察到澄清石灰水变浑浊和________的现象,说明气体产物是CO2和CO的混合物.
Ⅱ.首先对C和CuO反应的固体产物进行了探究.以下是他们进行实验后的实验报告,请你仔细阅读后完成相关的报告内容
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| 取7.2g红色固体,置于烧杯中,向其中加入足量稀硫酸,充分搅拌,静置. | 若无现象. | 证明红色固体是________. |
| 若有________, ________现象. | 证明红色固体肯定含有________,可能含有________. | |
| 取上述反应液过滤、洗涤、干燥和称量,得固体6.8g. | 确认红色固体是________.(写出详尽的计算过程) |
