题目内容
20.下列金属在空气(或氧气)中燃烧,生成物是黑色固体的是( )| A. | 镁带 | B. | 碳 | C. | 铁丝 | D. | 铝 |
分析 根据镁带、碳、铁丝、铝在氧气中燃烧的现象进行分析判断.
解答 解:A、镁条在氧气中燃烧,产生一种白色固体,故选项错误;
B、碳在氧气中燃烧,生成能使澄清石灰水变浑浊的气体,且碳不是金属,故选项错误;
C、铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体,故选项正确;
D、铝在氧气中燃烧,产生一种白色固体,故选项错误;
故选项为:C.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答;在描述物质燃烧的现象时,需要注意生成物的颜色、状态.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.为除去下列物质中的杂质(括号内为杂质),选用的试剂和操作方法都正确的是( )
| 序号 | 物 质 | 选用试剂(过量) | 操作方法 |
| A | Cu(Fe) | CuSO4溶液 | 加入CuSO4溶液,充分反应后过滤 |
| B | CO2(H2O) | 氧化钙 | 混合气体通过盛有氧化钙的U型管 |
| C | NH3(H2O) | 浓硫酸 | 混合气体通过有浓硫酸的洗气瓶 |
| D | NaOH溶液[Ca(OH)2溶液] | CO2气体 | 通入CO2气体充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
11.酸和碱的知识是九年级化学学习的重要知识.请回答下列有关问题:
(1)下列说法中不正确的是BD.(填字母代号)
A.酸和碱都含有氢元素 B.生成盐和水的反应一定是中和反应
C.多数酸和碱有腐蚀性 D.酸和碱能与所有的盐发生复分解反应
(2)为探究酸、碱的化学性质,某小组做了如图所示实验.
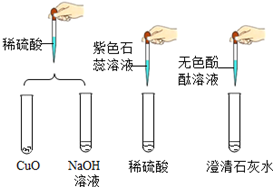
I、实验后某试管中为红色溶液,向其中加入一定量的某溶液后,红色消失变为无色,该反应的化学方程式为2HCl+Ca(OH)2═CaCl2+2H2O.
II、实验结束后,将得到的蓝色溶液和无色溶液倒入同一个干净的烧杯中,可观察到有蓝色沉淀生成,解释其原因?2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
(3)某敞口放置的氢氧化钠溶液已变质,用方程式表示其变质的原因2NaOH+CO2═Na2CO3+H2O.
为证明该瓶氢氧化钠溶液未完全变质,设计了以下实验,请将表格填写完整.
(1)下列说法中不正确的是BD.(填字母代号)
A.酸和碱都含有氢元素 B.生成盐和水的反应一定是中和反应
C.多数酸和碱有腐蚀性 D.酸和碱能与所有的盐发生复分解反应
(2)为探究酸、碱的化学性质,某小组做了如图所示实验.

I、实验后某试管中为红色溶液,向其中加入一定量的某溶液后,红色消失变为无色,该反应的化学方程式为2HCl+Ca(OH)2═CaCl2+2H2O.
II、实验结束后,将得到的蓝色溶液和无色溶液倒入同一个干净的烧杯中,可观察到有蓝色沉淀生成,解释其原因?2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
(3)某敞口放置的氢氧化钠溶液已变质,用方程式表示其变质的原因2NaOH+CO2═Na2CO3+H2O.
为证明该瓶氢氧化钠溶液未完全变质,设计了以下实验,请将表格填写完整.
| 实验操作 | 现象 | 结论 |
| 取少量该样品,滴入足量的 CaCl2溶液,充分反应后过滤. | 有白色沉淀生成 | 有关反应的化学方程式: CaCl2+Na2CO3═CaCO3↓+2NaCl |
| 在滤液中,滴入几滴 无色酚酞试液 | 溶液变红 | 样品未完全变质,仍含有氢氧化钠. |
5.在碳还原氧化铜和一氧化碳还原氧化铜这两个实验中,下列叙述不正确的是( )
| A. | 都能观察到黑色物质变成红色 | B. | 氧化铜都是氧化剂 | ||
| C. | 澄清石灰水都变浑浊 | D. | 都是置换反应 |
12.写出下列溶液中的溶质、溶剂或溶液的名称:
| 溶液 | 盐酸 | 澄清石灰水 | 碘酒 | ||
| 溶质 | 氯化钠 | 氢氧化钠 | |||
| 溶剂 | 水 | 水 |
9.下列物质在敞口容器中久置,质量增加的是( )
| A. | 浓硫酸 | B. | 浓盐酸 | C. | 稀硫酸 | D. | 汽水 |
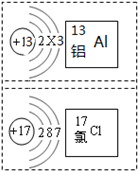 如图是铝和氯两种元素的有关信息,根据图示回答有关问题:
如图是铝和氯两种元素的有关信息,根据图示回答有关问题: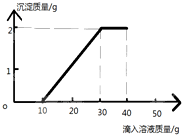 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取62.44g该混合溶液于烧杯中,向烧杯中滴入溶质质量分数为13.8%K2CO3溶液40克.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取62.44g该混合溶液于烧杯中,向烧杯中滴入溶质质量分数为13.8%K2CO3溶液40克.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求: