题目内容
日常生活中,人们利用碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好。下面是对影响碳酸钠溶液碱性的因素展开探究。
用碳酸钠固体和不同温度的水,配置溶质质量分数分别为2%、6%和10%的碳酸钠溶液,立即测量溶液的pH,记录数据如下表:
实验编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
水的温度/℃ | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 60 |
溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
请你分析表中数据回答:
(1)去油污的效果最好的是___________(填实验编号)。
(2)在一定温度范围内,温度对碳酸钠溶液pH的影响是:当碳酸钠溶液的质量分数相同时,_________。
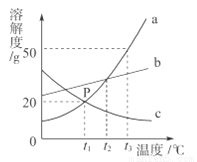
(3)要画出碳酸钠溶液的pH随溶液中溶质质量分数的变化关系曲线,可选择的一组实验是___________(填实验编号),结论是___________。
(4)如果某实验小组想得到更好的去污效果,根据之前的实验规律,可以尝试的实验条件是___________。
A.12%、60℃ B.8%、40℃ C.10%、70℃
(5)该小组配制50g 10% Na2CO3溶液的流程图如下所示:

该小组应称量Na2CO3的质量为__________g,若称量Na2CO3固体时指针向右偏转,则应____________________________直到天平平衡.
⑨ 温度越高,pH越大 ①④⑦或③⑥⑨ 在一定的温度下(或说其他条件相同时),当碳酸钠溶液的溶质质量分数越高,得到的溶液pH值越高 AC 5g 用药匙往左盘加入少量碳酸钠 【解析】根据所学知识和题中信息知,碳酸钠溶液具有碱性,清洗餐具上的油污,碱性越强,去油污的效果越好。(1)去油污的效果最好的是⑨,⑨溶液溶质质量分数最高,碱性最强。(2)在一定温度范围内,温度对碳酸钠溶液pH的影响是:当碳... 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案化学兴趣小组对“锌与稀硫酸反应快慢的影响因素”进行了探究。
(提出问题)锌与稀硫酸反应的快慢受哪些因素的影响呢?
(猜想与假设)①可能与稀硫酸的溶质质量分数有关;②可能与锌的形状有关。
(设计并实验)兴趣小组用100mL不同质量分数的稀硫酸和5g不同形状的锌进行如下实验(时间为3分钟)。
编号 | 硫酸的质量分数 (均取20mL) | 锌的形状 (均取1g) | 氢气的体积(mL) (均收集3分钟) |
1 | 20% | 锌粒 | 31.7 |
2 | 20% | 锌片 | 50.9 |
3 | 30% | 锌粒 | 61.7 |
4 | 30% | 锌片 | 79.9 |
(1)锌与硫酸反应的化学方程式为__________________________________。
(2)下图所示装置收集并测量氢气的体积,则正确的链接顺序是:氢气→_______________(填导管口序号)。

(收集证据)
(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是______。
(得出结论)依据上表得出的结论是____________________________________。
(反思评价)
(4)下表是兴趣小组第①组实验根据前6分钟记录详细数据(每分钟记录一次产生氢气的体积)。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积/mL | 3.1 | 16.7 | 11.9 | 9.6 | 7.6 | 6.0 |
请解释锌与稀硫酸反应由快变慢的原因____________________________________。
(5)锌与硫酸反应的快慢可能还会受_____________因素影响,如果用实验验证该因素对反应快慢的影响,应该控制________________因素不同,而其他因素则相同。
Zn + H2SO4 = ZnSO4 + H2↑ 0.4g e f g 1和3或2和4 相同条件下,硫酸的质量分数越大,反应速率越快或锌与硫酸的接触面积越大,反应速率越快 随着硫酸被消耗,硫酸溶质质量分数变小,所以反应速度由快变慢 温度 【解析】(1)锌与硫酸反应的化学方程式为: Zn + H2SO4 = ZnSO4 + H2 ↑ (2).当剩余的水较少时,水易从f端出来,故连接顺序是 e ...