题目内容
7.往硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生,根据上述现象你得到的结论是( )| A. | 滤渣中一定有铁粉 | B. | 滤渣中一定有铜粉和银粉 | ||
| C. | 滤渣中可能有银粉 | D. | 滤渣中可能有铜粉,一定有银粉 |
分析 铁比铜活泼,铜比银活泼,往硝酸银和硝酸铜的混合溶液中加入一定量的铁粉时,铁先和硝酸银反应生成硝酸亚铁和银,如果硝酸银完全反应后铁过量,则铁再和硝酸铜反应生成硝酸亚铁和铜.
解答 解:A、充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生,说明铁完全反应,滤渣中不含有铁粉,该选项说法不正确;
B、因为铁先和硝酸银反应,因此滤渣中一定含有银,如果铁不足或恰好和硝酸银反应,则硝酸铜不反应,滤渣中不含有铜,该选项说法不正确;
C、因为铁先和硝酸银反应,因此滤渣中一定含有银,该选项说法不正确;
D、因为铁先和硝酸银反应,因此滤渣中一定含有银,滤渣中可能有铜粉,例如铁和硝酸银反应后过量,则铁和硝酸铜反应生成硝酸亚铁和铜,该选项说法正确.
故选:D.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
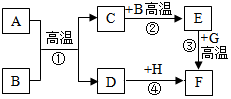
17.工业上常用高炉来进行炼铁,其原理如下.

(1)用CO和赤铁矿(Fe2O3)炼铁的化学反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)请从A或B两题中任选一个作答,若两题都作答,按A计分.

(1)用CO和赤铁矿(Fe2O3)炼铁的化学反应方程式是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)请从A或B两题中任选一个作答,若两题都作答,按A计分.
| A | B |
| 用含氧化铁160t的赤铁矿炼铁,理论上可以制得纯铁112t. | 工业上也常用主要成分为四氧化三铁的磁铁矿做炼铁原料.四氧化三铁中铁元素的质量分数计算式为$\frac{56×3}{56×3+16×4}$×100%. |
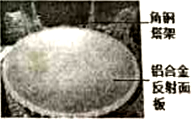 被誉为“中国天眼”的FAST,是目前世界上最大单口径,最灵敏的射电望远镜,2016年9月在贵州落成.如图所示,请完成下列各题
被誉为“中国天眼”的FAST,是目前世界上最大单口径,最灵敏的射电望远镜,2016年9月在贵州落成.如图所示,请完成下列各题