题目内容
20.下列说法不正确的是( )| A. | 用红磷测定空气中氧气含量时,红磷一定要过量 | |
| B. | 用排水法收集氧气时,导管口刚有气泡冒出就收集气体 | |
| C. | 硫粉在氧气中燃烧时,能产生有刺激气味的二氧化硫 | |
| D. | 实验室用过氧化氢制氧气的反应中,二氧化锰起催化作用 |
分析 A、根据用红磷测定空气中氧气含量实验的注意事项分析;
B、根据用排水法收集氧气时的注意事项分析;
C、根据做硫粉在氧气中燃烧实验时的注意事项分析;
D、根据实验室用过氧化氢制氧气实验中二氧化锰的作用分析.
解答 解:
A、用红磷测定空气中氧气含量时,为了消耗掉所有的氧气,红磷一定要过量,故说法正确;
B、用排水法收集氧气时,当导管口连续、均匀的冒出气泡时开始收集气体,否则收集的不纯,故说法错误;
C、硫粉在氧气中燃烧时生成二氧化硫,二氧化硫有毒,和水反应,因此集气瓶中放少量水可吸收二氧化硫,以防污染环境,故说法正确;
D、实验室用过氧化氢制氧气的反应中,二氧化锰在反应前后质量和化学性质没有改变,起催化作用,故说法正确;
故选B.
点评 本题考查知识点较多,综合性强,但只要掌握常见实验的注意事项即可解答.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
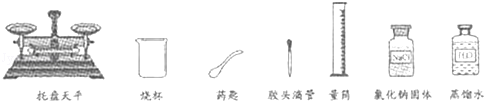
11.甲、乙、丙、丁四位同学在实验室里进行如下操作,其中正确的是( )
| A. | 甲做完实验后,将剩余的试剂倒回原试剂瓶 | |
| B. | 乙在点燃酒精灯时,用燃着的酒精灯引燃另一只酒精灯 | |
| C. | 丙在取稀盐酸时,在无用量说明的情况下,量取了1-2mL | |
| D. | 丁直接用手将粉末状药品加入试管中 |
8.图为甲、乙两种物质的溶解度曲线,从图中可获得正确信息的是( )
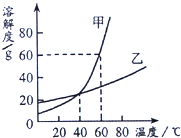

| A. | 40℃时,甲和乙物质的溶解度相同 | |
| B. | 升高温度可使不饱和的甲溶液变为饱和 | |
| C. | 60℃时,溶液甲的浓度大于乙 | |
| D. | 甲的溶解度大于乙的溶解度 |
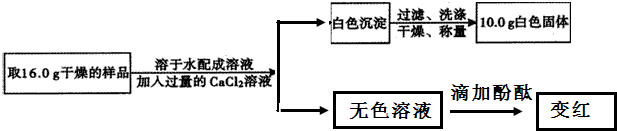
 小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.实验完毕后,称得所得固体的质量小于4.0g.
小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.实验完毕后,称得所得固体的质量小于4.0g.