题目内容
20.下列四个图象分别对应四种操作过程,其中不正确的是( )| A. | 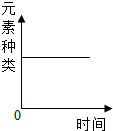 一定质量的镁在密闭的容器内燃烧 | |
| B. |  向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液 | |
| C. | 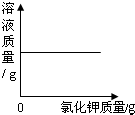 在室温下,向一定量的食盐饱和溶液中不断加入氯化钾晶体 | |
| D. | 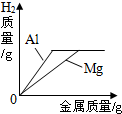 向等质量、等质量分数的稀硫酸中分别加入镁和铝 |
分析 A、根据质量守恒定律来解答该题;
B、盐酸和氯化钙的混合溶液的pH值小于7,而碳酸钠溶液的pH值大于7,可以据此解答该题;
C、向氯化钠溶液中加入氯化钾,氯化钾会继续溶解,而溶液质量也会随着增加,可以据此答题;
D、等质量等质量分数的稀硫酸中含有的氢元素的质量相等,而镁的活动性比铝的强,所以据此来解答该题.
解答 解:A、根据质量守恒定律,反应前后元素的种类不变,故正确;
B、盐酸和氯化钙的混合溶液的pH值小于7,碳酸钠的pH值大于7,同时碳酸钠可以和盐酸、氯化钙反应,所以当向其中加入碳酸钠溶液时,因为碳酸钠和氯化钙反应生成的碳酸钙能够溶于稀盐酸,所以碳酸钠要先和盐酸反应,由于发生了反应而使溶液的pH值增大,直至它们恰好完全反应时,溶液的pH值为7,继续加入碳酸钠则碳酸钠由于和氯化钙反应生成了沉淀,溶液的pH值不变,直至氯化钙被完全反应掉;继续滴加碳酸钠溶液,则溶液的pH值要大于7,即乙图为向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液,故B的图象和对应的操作相符;
C、室温下是食盐的饱和溶液,但是对于氯化钾来说是不饱和的溶液,即仍然可以溶解氯化钾,所以溶液的质量会继续增加,直至氯化钾也到达饱和状态,故C的图象和对应的操作不相符;
D、足量的金属与等质量、等质量分数的稀硫酸反应时生成氢气的质量是相等的,因为质量相等的同浓度的稀硫酸中氢元素的质量相等,所以最终生成氢气的质量是相等的,此时我们可以设生成氢气的质量为1g;
设生成1g氢气需铝的质量为x
2Al+3H2SO4═Al2(SO4)3+3H2↑
54 6
x 1g
$\frac{54}{6}=\frac{x}{1g}$
解得:x=9g
设生成1g氢气需要镁的质量为y
Mg+H2SO4═MgSO4+H2↑
24 2
y 1g
$\frac{24}{2}=\frac{y}{1g}$
解得 y=12g
所以经过计算可以得出生成等质量的氢气需要镁的质量更多,故D的图象和对应的操作相符.
故选C.
点评 熟练掌握电解水的实验现象及结论,能够根据溶液的性质来判断溶液的pH值的变化,同时熟练掌握金属的活动性顺序及其应用.

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案 “双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,设计实验进行探究.
“双吸剂”是常用的袋装食品的保鲜剂,可用来吸收氧气、二氧化碳、水蒸气等气体.某化学小组的同学在袋装食品中发现一包名为“504双吸剂”的保鲜剂,其标签如图所示.同学们对这包久置的“504双吸剂”的固体样品很好奇,设计实验进行探究.【提出问题】:久置固体的成分是什么?
【收集资料】:
(1)查阅资料:铁与氯化铁溶液在常温下生成氯化亚铁:Fe+2FeCl3═3FeCl2
(2)打开固体包装观察:部分粉末呈黑色、部分粉末呈白色、另有少数红棕色的块状固体.
【作出猜想】:久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.你猜想固体中可能含有Fe2O3的依据是:有少数红棕色的块状固体.
【实验探究】:如表是甲组同学设计并记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| 一、取少量固体加入足量蒸馏水,搅拌溶解 | 固体部分溶解,并放出大量热 | 固体中一定含有CaO |
| 二、过滤,取滤液滴加无色酚酞试液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
| 三、取滤渣加入足量稀盐酸 | 固体逐渐消失,产生大量无色气体,得到浅绿色溶液 | 固体中一定含有铁粉,一定不含有Fe2O3 |
| 四、将操作三中产生的气体通入到澄清石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
【继续探究】:为验证固体中是否含有Fe2O3,乙组同学用磁铁先分离出铁粉,向残留固体中加入足量稀盐酸,若溶液呈棕黄色,证明固体中含有Fe2O3.写出溶液呈棕黄色的化学反应方程式Fe2O3+6HCl=2FeCl3+3H2O.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | T1 | T2 | T3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色;反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂.
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
| A. | 烧碱 | B. | 纯碱 | C. | 精制粗盐 | D. | 尿素 |
| A. | 分子大,原子小 | |
| B. | 分子、原子在化学反应中都可以再分 | |
| C. | 分子、原子的质量和体积都非常小 | |
| D. | 分子可以构成物质,而原子不能构成物质 |
