题目内容
3.化学知识的整理和归纳对于化学的学习非常重要,以下归纳和推理正确的是( )| A. | 某溶液使酚酞溶液变红,该溶液一定是碱溶液 | |
| B. | 氧化物中含有氧元素,但含有氧元素的化合物不一定是氧化物 | |
| C. | 分子可以构成物质,所以物质都是由分子构成的 | |
| D. | 二氧化碳的大量排放会增强地球的温室效应,所以二氧化碳是空气污染物 |
分析 A、根据显碱性的不一定是碱溶液,如碳酸钠是盐解答;
B、根据氧化物的定义解答;
C、根据构成物质的基本粒子有分子原子和离子解答;
D、根据二氧化碳不是空气污染物解答.
解答 解:
A.显碱性的不一定是碱溶液,如碳酸钠是盐,其水溶液也显碱性,故A错;
B.氧化物中含有氧元素,含有氧元素的化合物不一定就是氧化物,例如NaOH不是氧化物,故B对;
C.构成物质的基本粒子有分子原子和离子,故C错;
D.二氧化碳的大量排放会增强地球的温室效应,但二氧化碳不是空气污染物,故D错.
故选B.
点评 本题主要考查溶液的酸碱性;从组成上识别氧化物,物质的构成.难度不大,熟练掌握有关知识,可以正确解答.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
13.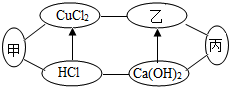 图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件己略去).下列说法中,正确的是 ( )
图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件己略去).下列说法中,正确的是 ( )
 图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件己略去).下列说法中,正确的是 ( )
图中甲、乙、丙是初中化学中常见的物质,图中“-”表示相连的物质之间可以在溶液中发生反应,“→”表示由某种物质可转化为另一种物质(部分反应物、生成物及反应条件己略去).下列说法中,正确的是 ( )| A. | 甲,乙,丙可能依次为Fe、NaOH、CO2 | |
| B. | 丙物质只能是氧化物或盐 | |
| C. | 当乙为NaOH时,它可由Ca(OH)2与Na2CO3反应生成 | |
| D. | 当甲为一种碱时,它与氯化铜溶液的反应一定产生两种沉淀 |
14.下列关于化学与人体健康说法正确的是( )
①霉变的粮食用来加工成家禽饲料;
②青少年要增加钙元素的摄入量;
③缺碘易引起坏血病;
④食用加铁酱油预防缺铁性贫血;
⑤用地沟油炸油条.
①霉变的粮食用来加工成家禽饲料;
②青少年要增加钙元素的摄入量;
③缺碘易引起坏血病;
④食用加铁酱油预防缺铁性贫血;
⑤用地沟油炸油条.
| A. | ①②③ | B. | ②④ | C. | ①②③④ | D. | ①③④ |
11.下列有关实验现象的描述不正确的是( )
| A. | 在滴有酚酞的烧碱溶液中滴加过量稀盐酸,溶液由红色变成无色 | |
| B. | 在空气中点燃镁条,发出耀眼的强光,生成白色固体 | |
| C. | 向鸡蛋清溶液中加饱和硫酸铵溶液有沉淀析出 | |
| D. | 水通电时正极产生的气体燃烧发出淡蓝色火焰 |
18.安徽的特色小吃品种繁多,历史悠久,独具地方特色.下面几个地市的著名特色小吃中所含 营养物质维生素较多的是( )
| A. | 符离集的烧鸡 | B. | 阜阳枕头馍 | C. | 庄墓荠菜圆子 | D. | 八公山豆腐 |
8.2016年1月24日,全国迎来30年一遇寒潮,广东省大部分地区下起了雪花!在寒冷天气里,人们必须摄取足够的食物,以维持体温和健康.下列有关说法中正确的是( )
| A. | 人体缺钙易引起甲状腺肿大 | |
| B. | 蛋白质、糖类、油脂都属于有机物,在体内消化会放出热量,维持体温 | |
| C. | 缺锌会引起食欲不振,生长迟缓,发育不良,因此我们要大量补充葡萄糖酸锌 | |
| D. | 摄入过多的油脂容易引发肥胖和心脑血管疾病,因此我们不要吃油脂类食物 |
15.某实验小组的同学要探究酸碱盐中碳酸钠的化学性质,设计了如下实验装置及方案:
(一)(1)步骤①中气球变瘪的原因碳酸钠与稀盐酸反应生成CO2,内部压强大于大气压;
(2)步骤①、②可得出碳酸钠具有与盐酸反应生成CO2的性质;
(3)步骤④的操作是将注射器4稍稍向外拉,其目的是证明CO2完全被吸收;
(4)步骤⑤中发生反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(5)步骤③④⑤可得出碳酸钠具有与含Ca2+的溶液反应生成白色沉淀的性质;
(二)上述实验结束后,实验小组的同学又对瓶内溶液的成分十分好奇,进行了探究:
(1)【提出猜想】通过分析,一致认为瓶内溶液的溶质中一定含有NaOH和NaCl,可能含有氢氧化钙或Na2CO3.
(2)【实验验证】设计实验方案确定溶液中溶质的组成.
(3)【反思与交流】根据所学化学知识,除了以上方案外,下列哪些物质可以代替试管B中加入的Na2CO3溶液完成该实验?ae(填序号)
a.K2CO3 b.BaCO3 c.CO2 d.无色酚酞 e.CuSO4.
| 实验装置 | 实验步骤及操作 | 实验现象 |
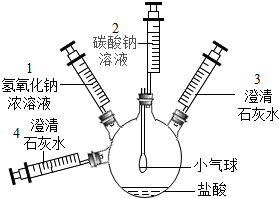 | ①将注射器2中的溶液推入盛有稀盐酸的瓶中,至不再有气泡产生. | 气球变瘪 |
| ②将注射器3稍稍向外拉 | 澄清石灰水变浑浊 | |
| ③将注射器1中的溶液推入瓶中 | 气球鼓起 | |
| ④将注射器4稍稍向外拉 | 无明显现象 | |
| ⑤将注射器4中的溶液推入瓶中 | 产生白色沉淀 |
(2)步骤①、②可得出碳酸钠具有与盐酸反应生成CO2的性质;
(3)步骤④的操作是将注射器4稍稍向外拉,其目的是证明CO2完全被吸收;
(4)步骤⑤中发生反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(5)步骤③④⑤可得出碳酸钠具有与含Ca2+的溶液反应生成白色沉淀的性质;
(二)上述实验结束后,实验小组的同学又对瓶内溶液的成分十分好奇,进行了探究:
(1)【提出猜想】通过分析,一致认为瓶内溶液的溶质中一定含有NaOH和NaCl,可能含有氢氧化钙或Na2CO3.
(2)【实验验证】设计实验方案确定溶液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量溶液于A、B两支试管中,A中 加入CaCl2溶液,B中加入Na2CO3溶液 | A中产生白色沉淀,B中没有沉淀 | 瓶内溶液中溶质的成分为NaOH、NaCl和Na2CO3 |
a.K2CO3 b.BaCO3 c.CO2 d.无色酚酞 e.CuSO4.
13.下列关于碳和碳的氧化物的说法错误的是( )
| A. | 石墨和金刚石都是由碳原子直接构成的单质 | |
| B. | 二氧化碳可用于光合作用、灭火、人工降雨等 | |
| C. | 一氧化碳能与血液中的血红蛋白结合导致中毒 | |
| D. | 一氧化碳和二氧化碳的性质用途的差异较大,是因为组成它们的元素种类不同 |