��Ŀ����
ͬѧ����̼������Һ������ķ�Ӧ��֤�����غ㶨�ɣ�ʵ������ǶԲ�����Һ�ijɷֽ���̽����
���������衿
 �����������ʷ�����Ӧ�Ļ�ѧ����ʽΪ ���ɴ��Ʋ����Һ��һ����NaCl��������Na2CO3�����ᡣ
�����������ʷ�����Ӧ�Ļ�ѧ����ʽΪ ���ɴ��Ʋ����Һ��һ����NaCl��������Na2CO3�����ᡣ
��ʵ��̽����
��1��ȷ����Һ���Ƿ������
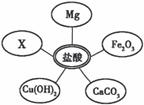
��ѡ���Լ�����������Ļ�ѧ���ʣ�ͬѧ��ѡ������ͼ��ʾ���������ʣ���������X�����ָʾ���е� ��Һ��
��ʵ����֤��ijͬѧ���Һ�м���������þ�ۣ��۲쵽 ��ȷ����Һ��һ��û�����ᡣ
��2��ȷ����Һ���Ƿ���Na2CO3��ijͬѧѡ�� �����Һ��pH=l0��
ȷ����Һ��һ������Na2CO3��
��3��������Һ���������ã����ӷ�Һ�еõ�������NaCl�����������ʵ�鷽����ơ�
| ���� | �����Լ� | �ᴿ�ķ��� | �������� |
| һ | ����Ca(NO3)2��Һ | ���ˡ������ᾧ | ��ѡ����л��У� |
| �� | �Թ����� |
| ���� |
��4����չ���ã�
������ͼ��������BaCl2��NaCl�Ĺ�������ʱ������Һ�������� ��
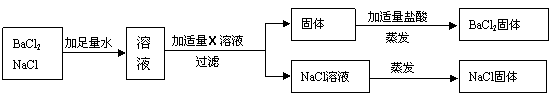 |
���������衿Na2CO3��2HCl��2NaCl��H2O��CO2��
��ʵ��̽�����Ţ�ʯ�� ��û�����ݲ��� ��pH��ֽ��pH��
��һ�������� ������������ᾧ ��Na2CO3

 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д����ǹ��ɻ�ѧ���ʵĻ��������ж�����������ȷ���ǣ�������
| �� | A�� | ����̼ԭ�ӹ��ɵ��������ڴ����� |
| �� | B�� | ԭ����һ���������ӡ����ӡ����� |
| �� | C�� | NaCl�������ӹ��ɵģ�����HClҲ�������ӹ��ɵ� |
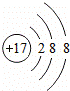
| �� | D�� | Cl�������ӽṹʾ��ͼΪ |
�����й�����ʹ�û���;����������ȷ���ǣ�������
| �� | A�� | ������ƽ������ʱ�ѳ�����������̣������������ |
| �� | B�� | ��ͷ�ιܣ����Թ��еμ�Һ��ʱӦ����ͷ�ι������Թ��� |
| �� | C�� | �ƾ��ƣ�Ϩ��ƾ���ʱ�����촵�� |
| �� | D�� | �Թܣ�����ʱ��ʢҺ����� |
 ���ó����Թ��ݻ���
���ó����Թ��ݻ���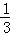
 �ס������ֹ������ʵ��ܽ�����ߡ�����˵��������� ��������
�ס������ֹ������ʵ��ܽ�����ߡ�����˵��������� ��������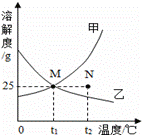

 ��� D��ԭ�ӵ���ը
��� D��ԭ�ӵ���ը