题目内容
18.金属钠及其部分化合物的化学性质比较活泼,保存不当较易变质,请你根据所学知识回答下列问题:
(1)如图1是金属钠在元素周期表中的信息,下列关于钠元素的说法不正确的是C
A.钠属于金属元素 B.钠的核电荷数为11
C.相对原子质量为22.99g D.原子核外有11个电子
(2)过氧化钠(Na2O2)遇到水会发生反应:2Na2O2+2H2O=4NaOH+x↑,请写出x的化学式O2.
(3)为了验证实验室保存的NaOH是否变质,某同学设计了如图2所示实验方案进行探究,请据图回答:
①实验中测定溶液pH的方法是用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH.
②氢氧化钠变质的原因是2NaOH+CO2═Na2CO3+H2O (用化学方程式表示),根据实验现象,你认为该氢氧化钠固体已变质(填“已”或“未”).
③实验中加入过量氯化钡溶液的目的是使碳酸钠完全反应.
④若测得溶液E的pH>7,则样品A的成分是氢氧化钠和碳酸钠.
(4)取已变质的氢氧化钠样品配制成100g溶液,向其中加入溶质质量分数为7.3%的稀盐酸100g,完全反应后得到中性溶液197.8g.
试计算所取样品中含杂质碳酸钠的质量.
分析 (1)根据图中提供的信息可以判断相关方面的问题;
(2)化学反应前后,元素种类不变,原子种类和总个数不变;
(3)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
碳酸钠溶液和氢氧化钠溶液都是显碱性的溶液,pH大于7;
(4)根据提供的数据和反应的化学方程式可以进行相关方面的计算和判断.
解答 解:(1)A.钠属于金属元素,该选项说法正确;
B.钠的核电荷数为11,该选项说法正确;
C.相对原子质量的单位不是g,该选项说法不正确;
D.原子核外有11个电子,该选项说法正确.
故选:C.
(2)反应前后钠原子都是4个,氢原子都是4个,反应前氧原子是6个,反应后应该是6个,其中2个包含在x中,因此x的化学式是O2.
故填:O2.
(3)①实验中测定溶液pH的方法是:用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH.
故填:用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH.
②氢氧化钠变质的原因是氢氧化钠和二氧化碳反应生成了碳酸钠和水,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
根据实验现象可知,滴加稀盐酸时产生气泡,说明溶液中含有碳酸钠,进一步说明该氢氧化钠固体已经变质.
故填:2NaOH+CO2═Na2CO3+H2O;已.
③实验中加入过量氯化钡溶液的目的是使碳酸钠完全反应,避免对检验氢氧化钠产生干扰.
故填:使碳酸钠完全反应.
④若测得溶液E的pH>7,说明溶液中含有氢氧化钠,则样品A的成分是氢氧化钠和碳酸钠.
故填:氢氧化钠和碳酸钠.
(4)设碳酸钠质量为x,
反应生成二氧化碳质量为:100g+100g-197.8g=2.2g,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 44
x 2.2g
$\frac{106}{x}$=$\frac{44}{2.2g}$,
x=5.3g,
所取样品中含杂质碳酸钠的质量是5.3g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

| A. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| B. | 在日常生活中,大量使用的常常不是纯金属,而是它们的合金 | |
| C. | 铜的化学性质不活泼,所以铜制品不会生锈 | |
| D. | “真金不怕火炼”说明黄金的硬度非常大 |
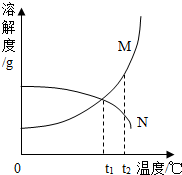 如图,M、N两种不含结晶水的固体物质的溶解度曲线.据图判断,下列说法中正确的是( )
如图,M、N两种不含结晶水的固体物质的溶解度曲线.据图判断,下列说法中正确的是( )| A. | M、N的溶解度都随温度的升高而增大 | |
| B. | 将t1℃时,M的饱和溶液升温至t2摄氏度,溶质的质量分数增大 | |
| C. | 在t1℃时,M、N的饱和溶液中溶质的质量分数二者相等 | |
| D. | 将t2℃时,M、N的饱和溶液分别降温至t1摄氏度,两溶液中均析出晶体 |
 如图实验室用高锰酸钾制氧气的装置图,现有五处错误,请指出并加以改正
如图实验室用高锰酸钾制氧气的装置图,现有五处错误,请指出并加以改正
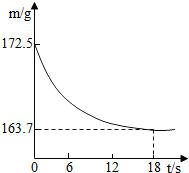 某公司生产出的纯碱产品中经检测只含有氯化钠杂质.为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液;反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示.
某公司生产出的纯碱产品中经检测只含有氯化钠杂质.为测定产品中碳酸钠的质量分数,20℃时,称取该产品样品26.5g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶液;反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图所示. 在对蜡烛及其燃烧进行了探究以后,请你填写下列空格:
在对蜡烛及其燃烧进行了探究以后,请你填写下列空格: