题目内容
16.从分子的角度分析并解释下列事实,说法正确的是BCA.水结成冰,是因为温度降低,分子停止运动
B.碘酒是混合物,是因为由不同分子构成的
C.干冰升华,是因为分子间间隔变大
D.一氧化碳有毒,二氧化碳没有毒,是因为分子的构成不同.
分析 A、根据分子的性质分析;
B、根据解答物质的微观构成粒子解答;
C、根据分子的性质解答;
D、根据分子的构成解答.
解答 解:A、分子是不断运动的,分子间有间隔,水结成冰是分子的间隔发生了变化,分子并没有停止运动,故A错误;
B、碘是由碘分子构成的,酒精是由酒精分子构成的,故碘酒是混合物,故B正确;
C、分子间有间隔,干冰升华,是因为分子间间隔变大,正故C确;
D、一氧化碳有毒,二氧化碳没有毒,是因为分子的构成不同.
故选:BC,D补充:分子的构成不同.
点评 本题考查的是物质的微观构成粒子的知识,掌握粒子的性质是正确解答本题的关键.

练习册系列答案
相关题目
7.某学校化学兴趣小组进行“Na2CO3和NaCl混合物中Na2CO3含量测定”的实验,设计了如下两种方案:
(1)请你帮助完成如表探究:
(2)假设在方案一:15g样品与100g稀HCl 恰好完全反应(烧杯质量为89.4g),充分反应后,称得烧杯和剩余物总质量为200g.试计算:
①生成CO2 的质量:15g+100g+89.4g-200g=4.4g(列式并写出结果);
②样品中Na2CO3 的质量分数;
③稀盐酸中溶质的质量分数.
(1)请你帮助完成如表探究:
| 方案 | 所选试剂 | 现象 | 化学方程式 |
| 方案一:测定反应后生成CO2的质量,计算出样品中Na2CO3的含量 | 稀盐酸 | 产生气泡 | Na2CO3+2HCl═ 2NaCl+H2O+CO2↑ |
| 方案二:测定反应后生成沉淀的质量,计算出样品中Na2CO3的含量 | 水、 氯化钙 | 产生白 色沉淀 |
①生成CO2 的质量:15g+100g+89.4g-200g=4.4g(列式并写出结果);
②样品中Na2CO3 的质量分数;
③稀盐酸中溶质的质量分数.
8.下列物质在氧气中燃烧现象的描述,正确的是( )
| A. | 硫燃烧发出淡蓝色火焰,放热,生成有刺激性气味的气体 | |
| B. | 红磷在氧气中燃烧产生白雾,放出大量的热 | |
| C. | 木炭燃烧生成黑色固体,倒入瓶中的澄清石灰水变浑浊 | |
| D. | 铁丝在氧气中燃烧火星四射,放热,生成黑色物质 |
8.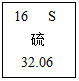 如图是硫元素在元素周期表中的信息示意图,从中获取的相关信息正确的是( )
如图是硫元素在元素周期表中的信息示意图,从中获取的相关信息正确的是( )
 如图是硫元素在元素周期表中的信息示意图,从中获取的相关信息正确的是( )
如图是硫元素在元素周期表中的信息示意图,从中获取的相关信息正确的是( )| A. | 硫的核电荷数是16 | B. | 硫的元素符号为“s” | ||
| C. | 硫原子的相对质量为32.6g | D. | 硫是金属元素 |
5.化学对人类生活和社会发展做出了巨大贡献.下列对知识归纳都正确的一组是( )
| A、生活常识 | B、物质鉴别 |
| 洗涤剂洗油污--乳化作用 铁生锈--用酒精清洗 | 食盐与亚硝酸钠--品尝 硬水与软水--肥皂水 |
| C、安全常识 | D、环境保护 |
| 油锅不慎着火--可以盖上锅盖灭火 火灾烟很大时--用湿毛巾捂住口鼻 | 减少白色污染--少使用塑料制品 减少酸雨污染--不使用化石燃料 |
| A. | A | B. | B | C. | C | D. | D |
6.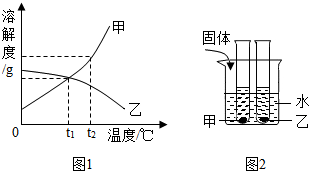 图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
 图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )| A. | t2℃时,甲、乙的饱和溶液中溶质的质量分数大小关系为甲>乙 | |
| B. | 甲、乙的饱和溶液分别从t2℃降至t1℃时,两溶液中溶质的质量分数大小关系为甲>乙 | |
| C. | 向烧杯的水中加NaOH固体后,乙溶液由饱和溶液变成不饱和溶液 | |
| D. | 向烧杯的水中加NH4NO3固体后,甲溶液溶质的质量分数减小 |

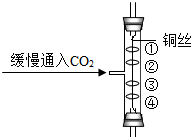 物质的用途与其性质密切相关.
物质的用途与其性质密切相关.