题目内容
15.某同学用一定浓度的稀硫酸与氧化铜反应,其5次实验结果如表所示:| 实验次别 | 氧化铜(g) | 硫酸溶液(mL) | 硫酸铜(g) |
| 1 | 2.0 | 120 | 4.0 |
| 2 | 4.0 | 120 | 8.0 |
| 3 | 6.0 | 120 | 9.6 |
| 4 | 8.0 | 200 | 16.0 |
| 5 | 10.0 | 300 | X |
(2)哪几次硫酸有剩余1、2、5.
(3)X=20g.
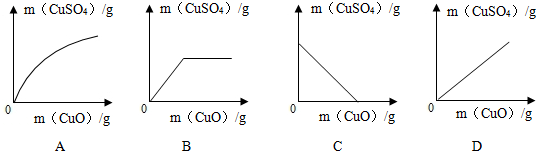
(4)若硫酸的用量一定,以反应物氧化铜的质量为横坐标,以生成物硫酸铜质量为纵坐标,则如图的函数图象B符合反映事实.
分析 根据表中提供的数据可以进行分析、判断,从而发现物质的变化规律,由1可知2.0g氧化铜可生成硫酸铜4g,所以可判断氧化铜的过量情况,酸有剩余即氧化铜完全反应后酸还有剩余的过程,利用表中的数据分析可完成相关的判断.
解答 解:由1、2、3次实验可知,每2g氧化铜完全反应会生成4g硫酸铜,而由2到4的实验硫酸铜的量增加的不成比例,也就是当酸足量时,6g氧化铜可生成12g硫酸铜,但却生成了9.6g,说明酸量不足,又因为由4g氧化铜变到6g氧化铜时,硫酸铜的量有所增加,所以120mL的硫酸在1、2步中一定会有剩余,所以3中氧化铜过量,硫酸已全部反应,因此120mL硫酸最多生成硫酸铜的质量是9.6g硫酸铜,4步中,200mL硫酸最多生成硫酸铜的质量是16g,结合2步中可知,4步中的硫酸和氧化铜是完全反应的,生成硫酸铜是16g,所以5步中硫酸是过量的,将氧化铜与2步比较可知,生成硫酸铜质量是20g.
当硫酸的量一定时,生成的硫酸铜也是一定的,即从反应开始硫酸铜的质量逐渐增加,到硫酸反应完时不再增加,故选:B.
故答案为:(1)3;
(2)1、2、5;
(3)20g;
(4)B.
点评 该题是对数据分析知识的考查,解题的关键是找到数据中反应的相关规律,是一道训练学生思维能力的综合知识考查题.

练习册系列答案
相关题目
5.二氧化锰可作过氧化氢分解的催化剂,兴趣小组的同学想探究过氧化氢分解有没有其他催化剂.
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
【实验结论】
(1)A试管中产生的气体是氧气.
(2)实验Ⅱ证明氧化铁的化学性质在反应前后没有发生变化.实验Ⅲ中如果a=1g,则证明氧化铁的质量在反应前后没有发生变化,可以作过氧化氢分解的催化剂.
(3)写出氧化铁催化过氧化氢分解的文字表达式:过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
【实验评价】实验设计Ⅳ的目的是比较氧化铁与二氧化锰对过氧化氢分解的催化效率,其中b=1g.若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰对过氧化氢的分解催化效率更高.
【实验拓展】查阅资料得知,氧化铜、硫酸铜、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂.下列有关催化剂的说法正确的是B.
A.二氧化锰只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.一个化学反应只有一种催化剂
D.用作催化剂的物质不可能是其他反应的反应物或生成物.
【提出问题】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
【实验探究】
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入1g氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
| Ⅲ.将实验中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量为ag | |
| Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入1g氧化铁粉末,向D试管中加入bg二氧化锰粉末,观察现象 |
(1)A试管中产生的气体是氧气.
(2)实验Ⅱ证明氧化铁的化学性质在反应前后没有发生变化.实验Ⅲ中如果a=1g,则证明氧化铁的质量在反应前后没有发生变化,可以作过氧化氢分解的催化剂.
(3)写出氧化铁催化过氧化氢分解的文字表达式:过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
【实验评价】实验设计Ⅳ的目的是比较氧化铁与二氧化锰对过氧化氢分解的催化效率,其中b=1g.若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是二氧化锰对过氧化氢的分解催化效率更高.
【实验拓展】查阅资料得知,氧化铜、硫酸铜、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂.下列有关催化剂的说法正确的是B.
A.二氧化锰只能作过氧化氢溶液分解的催化剂
B.同一个化学反应可以有多种催化剂
C.一个化学反应只有一种催化剂
D.用作催化剂的物质不可能是其他反应的反应物或生成物.
6.下列说法不正确的是( )
| A. | 酸中的水溶液一定含有氢离子 | B. | 碱中一定含有氢元素 | ||
| C. | 盐中一定含有氧元素 | D. | 酸和碱发生的反应一定有水生成 |
3.隔夜莱是否能吃,主要在于烧熟后的隔夜菜中亚硝酸盐含量的变化是否符合食品安全要求.蔬菜中的硝酸盐来自生长过程中所施氮肥.空气中的微生物(如硝酸盐还原菌)进入到蔬菜中,会产生一种还原酶,使蔬莱中的部分硝酸盐还原成亚硝酸盐.烧熟后的莱在食用和保存阶段都会有一些细菌进入;做熟的蔬菜更适合细菌生长.
某研究小组对烧熟的莱中亚硝酸盐含量做了测试,数据如下表:
盖有保鲜膜的菜肴在4℃的冰箱中放置不同时间的亚硝酸盐含量(单位:mg/kg)
将一份红烧鲫鱼样本(不盖保鲜膜)在常温下放置4小时,测定其亚硝酸盐含量为A8.9483mg/g.请根据以上材料,回答下列问题:
(1)亚硝酸盐中含有NO2-,其中氮元素的化合价是+3价.
(2)根据表中的数据,菜中的亚硝酸盐含量变化的共同规律是:菜中的亚硝酸盐含量随时间的增加而增加,温度高和不密封菜中的亚硝酸盐含量增加越快
(3)要使烧熟后的隔夜莱中亚硝酸盐含量尽可能低,保存的条件应该是低温和密封
(4)炒菜过程中温度一般在100℃以上,你认为从生菜炒到熟菜过程中的亚硝酸盐含量是否会持续增加不会,原因是高温条件下空气中的微生物(如硝酸盐还原菌)会被杀死.
某研究小组对烧熟的莱中亚硝酸盐含量做了测试,数据如下表:
盖有保鲜膜的菜肴在4℃的冰箱中放置不同时间的亚硝酸盐含量(单位:mg/kg)
| 菜肴 | 半小时 | 6小时 | 18小时 | 24小时 |
| 炒青菜 | 0.6861 | 0.7982 | 4.3333 | 5.3624 |
| 韭菜炒蛋 | 1.8153 | 1.9249 | 2.8390 | 5.6306 |
| 红烧肉 | 2.4956 | 4.2558 | 4.3668 | 5.5188 |
| 红烧鲫鱼 | / | 2.0948 | 3.2300 | 7.2397 |
(1)亚硝酸盐中含有NO2-,其中氮元素的化合价是+3价.
(2)根据表中的数据,菜中的亚硝酸盐含量变化的共同规律是:菜中的亚硝酸盐含量随时间的增加而增加,温度高和不密封菜中的亚硝酸盐含量增加越快
(3)要使烧熟后的隔夜莱中亚硝酸盐含量尽可能低,保存的条件应该是低温和密封
(4)炒菜过程中温度一般在100℃以上,你认为从生菜炒到熟菜过程中的亚硝酸盐含量是否会持续增加不会,原因是高温条件下空气中的微生物(如硝酸盐还原菌)会被杀死.
20.某物质4.6g,在氧气中完全燃烧,生成8.8g CO2和5.4g H2O,则该物质可能为( )
| A. | C2H5OH | B. | C2H2 | C. | CH4 | D. | C3H8 |
5.英国物理学家卢瑟福通过对α粒子散射实验的研究提出了原子的核式结构模型,该模型包括的内容不正确的有( )
| A. | 原子的中心有一个很小的原子核 | |
| B. | 原子的全部正电荷集中在原子核内 | |
| C. | 原子的质量几乎全部集中在原子核内 | |
| D. | 原子是由质子和中子的组成的 |
 氮化铝(AlN)是一种新型无机材料.某氮化铝样品中含有碳或氧化铝杂质.已知氮化铝和NaOH溶液能反应,其反应方程式为:
氮化铝(AlN)是一种新型无机材料.某氮化铝样品中含有碳或氧化铝杂质.已知氮化铝和NaOH溶液能反应,其反应方程式为: