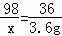题目内容
氢氧化铜、氢氧化铁、氢氧化锌的混合物若干,与10%的硫酸溶液完全反应,生成3.6g的水.则已反应的硫酸的质量为( )
|
| A. | 19.6 g | B. | 4.9 g | C. | 10.0 g | D. | 9.8 g |
| 根据氢氧化铜、氢氧化铁、氢氧化锌分别与硫酸反应的方程式找出硫酸与生成水的关系即可求出反应的硫酸的质量进行解答. | |
| 解答: | 解:设已反应的硫酸的质量为x. 氢氧化铜、氢氧化铁、氢氧化锌分别与硫酸反应的方程式分别为Cu(OH)2+H2SO4=CuSO4+2H2O、2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O、Zn(OH)2+H2SO4=ZnSO4+2H2O,可知硫酸与生成水的关系为 H2SO4 ~2H2O 98 36 x 3.6g
x=9.8g 故选:D. |

练习册系列答案
相关题目