题目内容
4.请根据如表回答有关问题:| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 水 | 熟石灰 | 纯碱 |
| 化学式 | CH3COOH | H2O | Ca(OH)2 | Na2CO3 |
(2)利用表中的物质作为反应物,写出一个制取氢氧化钠的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(3)若要测定纯碱溶液的酸碱度,可选用下列选项中的③.
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸.
分析 (1)碱是指电离时生成的阴离子全部是氢氧根离子的化合物,盐是指由金属离子和酸根离子组成的化合物,据此分析;
(2)根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式;
(3)实验室中可用pH试纸来测定溶液的酸碱度,根据测定酸碱度的方法分析.
解答 解:(1)氢氧化钙电离时生成的阴离子全部是氢氧根离子,属于碱;碳酸钠是由钠离子和碳酸根离子组成的化合物,属于盐.故答案为:③;④;
(2)碳酸钠和氢氧化钙反应能生成氢氧化钠和碳酸钙,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.故答案为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)测定溶液的酸碱度用pH试纸,具体的操作方法为:取一片pH试纸放在表面皿或玻璃片上,用玻璃棒或胶头滴管蘸取纯碱溶液滴在pH试纸上,变色后与标准比色卡对照,读出溶液的pH值.酚酞或石蕊只能测溶液酸碱性.故答案为:③.
点评 解答本题要掌握化学方程式的书写方法和物质的分类方法等方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
16.在倡导“节能环保”、“低碳生活”的今天,人类非常重视新能源的开发和利用.下列能源不属于新能源的是( )
| A. | 氢能 | B. | 石油 | C. | 太阳能 | D. | 风能 |
13.在厨房里发生的下列变化中,属于物理变化的是( )
| A. | 煤气燃烧 | B. | 瓷碗摔碎 | C. | 食物腐败 | D. | 面粉发酵 |
20.下列说法不正确的是( )
| A. | 盐酸可以用来除去铁锈 | |
| B. | 酸能使紫色石蕊试液变红色 | |
| C. | 氢氧化铜可以溶解在稀硫酸中 | |
| D. | 任何酸都能与氯化钡反应生成白色沉淀 |
11.小强同学分别取溶质质量分数相同的稀盐酸,大小、形状都相同的某种金属X、Al、Cu 进行实验,实验现象记录如表
回答下列问题:
(1)实验开始时,铝表面几乎无气泡产生的原因是铝表面的氧化铝和稀盐酸反应生成氯化铝和水.
(2)Cu表面始终无气泡产生的原因是铜不能和稀盐酸反应.
(3)三种金属的活动性由强到弱的顺序是Al>X>Cu.
(4)如果金属X的活动性比铁弱,且金属X与稀盐酸反应后生成易溶于水的XCl2.向只含有XCl2、CuCl2两种溶质的溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入稀盐酸,没有气泡产生.则滤液中一定含有的金属阳离子是Fe2+(用离子符号表示).
| Al | X | Cu | ||
| 现象 | 开始时 | 几乎无气泡产生 | 产生气泡速度慢 | 无气泡产生 |
| 一段时间后 | 产生气泡速度快 | 产生气泡速度慢 | 无气泡产生 |
(1)实验开始时,铝表面几乎无气泡产生的原因是铝表面的氧化铝和稀盐酸反应生成氯化铝和水.
(2)Cu表面始终无气泡产生的原因是铜不能和稀盐酸反应.
(3)三种金属的活动性由强到弱的顺序是Al>X>Cu.
(4)如果金属X的活动性比铁弱,且金属X与稀盐酸反应后生成易溶于水的XCl2.向只含有XCl2、CuCl2两种溶质的溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中加入稀盐酸,没有气泡产生.则滤液中一定含有的金属阳离子是Fe2+(用离子符号表示).
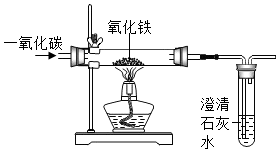 如图是用一氧化碳与氧化铁反应制取少量铁单质的装置图,请回答相关问题.
如图是用一氧化碳与氧化铁反应制取少量铁单质的装置图,请回答相关问题.