题目内容
10.大蒜中含有一种有效成分硫化丙烯(C3H6S)具有一定杀菌食疗的作用.下列有关硫化丙烯的说法正确的是( )| A. | 硫化丙烯的相对分子质量为74g | |
| B. | 硫化丙烯由3个碳原子、6个氢原子和1个硫原子构成 | |
| C. | 硫化丙烯中碳、氢、硫元素的质量比为3:6:1 | |
| D. | 硫化丙烯中碳元素的质量分数为48.6% |
分析 A.根据相对分子质量的单位来分析;
B.根据物质的结构来分析;
C.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行分析;
D.根据化合物中元素质量分数的计算方法来分析.
解答 解:A.相对分子质量的单位不是“g”而是“1”,通常省略,故错误;
B.硫化丙烯是由分子构成的,而不是由原子直接构成的,故错误;
C.硫化丙烯中碳元素、氢元素和硫元素的质量比为(12×3):(1×6):32≠3:6:1,故错误;
D.硫化丙烯中碳元素的质量分数为$\frac{12×3}{12×3+1×6+32}×100%$≈48.6%,故正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
20.如图所示,小明同学为了验证稀硫酸化学性质所做的三个实验,回答下列问题.
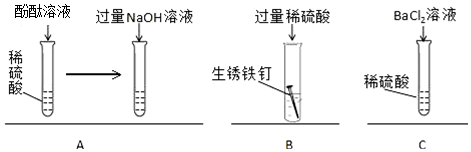
(1)A实验最终能观察到的现象是溶液由无色变红色;
(2)B实验中,将一只生锈的铁钉放入过量的稀硫酸中,铁钉表面的铁锈逐渐溶解,溶液变成黄色(填写实验现象);反应一段时间后,裸露在外的铁与稀硫酸接触进一步反应,有少量气泡产生,写出产生气泡这一变化的化学方程式Fe+H2SO4=FeSO4+H2↑,该反应在基本反应类型中属于置换反应(填基本反应类型),此时取出铁钉,发现铁钉光亮,溶液为黄绿色.
(3)将上述A、B实验后所得溶液在烧杯中混合,观察到烧杯底部有沉淀,上层为红色溶液,根据下表信息可知,过滤得到的溶液中存在的溶质为氢氧化钠、硫酸钠(除酚酞外);
(4)若将上述A、C实验后所得废液在烧杯中混合,请你设计实验证明混合溶液中有过量的BaCl2 存在,写出关键的实验操作及现象是取A实验后的溶液与C混合,若沉淀的质量增加,则证明实验中所加BaCl2溶液过量.

(1)A实验最终能观察到的现象是溶液由无色变红色;
(2)B实验中,将一只生锈的铁钉放入过量的稀硫酸中,铁钉表面的铁锈逐渐溶解,溶液变成黄色(填写实验现象);反应一段时间后,裸露在外的铁与稀硫酸接触进一步反应,有少量气泡产生,写出产生气泡这一变化的化学方程式Fe+H2SO4=FeSO4+H2↑,该反应在基本反应类型中属于置换反应(填基本反应类型),此时取出铁钉,发现铁钉光亮,溶液为黄绿色.
(3)将上述A、B实验后所得溶液在烧杯中混合,观察到烧杯底部有沉淀,上层为红色溶液,根据下表信息可知,过滤得到的溶液中存在的溶质为氢氧化钠、硫酸钠(除酚酞外);
| SO42- | OH- | |
| Fe3+ | 溶 | 不溶 |
| Fe2+ | 溶 | 不溶 |
18.生活中常见的几种“水”,可看作纯净物的是( )
| A. | 汽水 | B. | 蒸馏水 | C. | 自来水 | D. | 矿泉水 |
5.下列实验中,能达到相应目的是( )
| A. | 制备少量KOH溶液,K2CO3溶液与NaOH溶液混合后过滤 | |
| B. | 鉴别稀硫酸,NaOH溶液和KCl溶液,选用酚酞溶液 | |
| C. | 除去NaNO3溶液中混有的少量Na2CO3,滴加适量的BaCl2溶液,过滤 | |
| D. | 验证质量守恒定律,比较碳酸钠粉末和稀盐酸在烧杯中反应前和反应后的质量 |
20.下列物质属于纯净物的是( )
| A. | 石油 | B. | 干冰 | C. | 生铁 | D. | 糖水 |
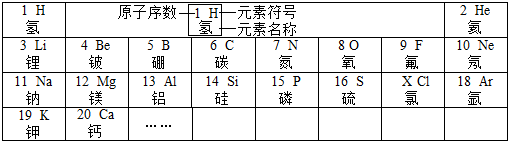
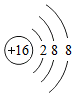 表示硫离子的结构示意图,请写出该离子的离子符号S2-.
表示硫离子的结构示意图,请写出该离子的离子符号S2-.