题目内容
7.下列图象与所属实验事实相符的是( )| A. | 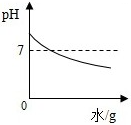 稀释NaOH溶液 | B. |  镁在空气中燃烧 | ||
| C. | 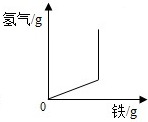 铁加入稀盐酸中 | D. | 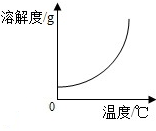 氧气的溶解度 |
分析 A.根据碱溶液加水稀释过程中,溶液pH的变化来分析;
B.根据化学反应中物质之间的质量关系来分析;
C.根据一定质量的盐酸与足量的铁反应生成氢气的质量来分析;
D.根据气体的溶解度与温度的关系来分析.
解答 解:A.氢氧化钠溶液显碱性,其pH大于7,加水稀释后碱性减弱,pH变小,但是溶液仍然显碱性,pH大于7,故错误;
B.镁与空气中的氧气反应生成氧化镁,随着镁的质量的增加,生成氧化镁的质量也会不断增加,故正确;
C.盐酸与铁反应生成氯化亚铁和氢气,当足量的铁与一定质量的盐酸反应时,生成氢气的质量当盐酸完全反应后质量不再增加,故错误;
D.气体的溶解度随着温度的升高而减小,故错误.
故选B.
点评 本题考查了酸碱的稀释、质量守恒定律、酸与金属的反应以及温度对气体溶解度的影响,难度不大.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
18.图l表示向一定量氯化钙和稀盐酸的混合溶液中滴加碳酸钠溶液,横坐标表示加入的碳酸钠溶液的质量,纵坐标表示实验中得到的沉淀或气体的质量;图2表示一定体积的气体X和不同体积的氧气反应(若反应生成水,水为液态),横坐标表示通入的氧气体积;纵坐标表示反应后气体的总体积(反应前、后的温度与压强相同.同温同压下,相同体积的任何气体含有相同的分子数).下列叙述中正确的是( )
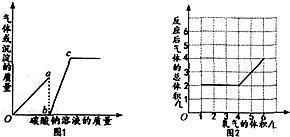

| A. | 图l中oa段表示实验中沉淀质置的变化情况 | |
| B. | 图l中c点表示上述混合溶液与碳破钠溶液恰好完全反应 | |
| C. | 由图2可知,反应前X的体积为2L | |
| D. | 由图2可知,x可能是C0或CH4 |
2.某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16克放入烧杯,把80克稀盐酸平均分成四份依次加入,测量过程所得数据见下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,也不与稀盐酸反应).请计算:
(1)上表中n的数值为2.8.
(2)样品中碳酸钙的质量分数为82.5%.
(3)请用图表示出滴加盐酸的质量与产生气体的质量之间的关系.(横坐标表示滴加盐酸的质量,纵坐标表示产生气体的质量)
(4)小明同学计算所用盐酸的溶质质量分数,计算过程如下:
解:设盐酸的溶质质量分数为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
13.2g 80x
100:73=13.2:80x
x=12%
小明的计算过程中存在明显错误,你能通过列式计算进行纠正吗?
| 序号 | 加入稀盐酸的质量/克 | 剩余固体的质量/克 |
| 第一次 | 20 | 11 |
| 第二次 | 20 | 6 |
| 第三次 | 20 | 2.8 |
| 第四次 | 20 | n |
(2)样品中碳酸钙的质量分数为82.5%.
(3)请用图表示出滴加盐酸的质量与产生气体的质量之间的关系.(横坐标表示滴加盐酸的质量,纵坐标表示产生气体的质量)
(4)小明同学计算所用盐酸的溶质质量分数,计算过程如下:
解:设盐酸的溶质质量分数为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
13.2g 80x
100:73=13.2:80x
x=12%
小明的计算过程中存在明显错误,你能通过列式计算进行纠正吗?
19.下列物质属于纯净物的是( )
| A. | 河水 | B. | 汽水 | C. | 蒸馏水 | D. | 矿泉水 |
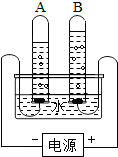 如图是实验室电解水的简易装置示意图.
如图是实验室电解水的简易装置示意图.