题目内容
请将下列变化用化学方程式表示,并按照要求填写正确答案.(1)二氧化碳通入澄清石灰水______;
(2)一氧化碳还原氧化铁______ 2Fe+3CO2
【答案】分析:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.
解答:解:(1)二氧化碳与氢氧化钙反应生成碳酸钙和水,Ca(OH)2+CO2═CaCO3↓+H2O;
(2)一氧化碳与氧化铁反应生成铁和二氧化碳,3CO+Fe2O3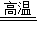 2Fe+3CO2;
2Fe+3CO2;
(3)铝和二氧化锰在高温条件下生成锰和氧化铝4Al+3MnO2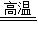 3Mn+2Al2O3;
3Mn+2Al2O3;
(4)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊变红,加热后碳酸分解生成水和二氧化碳,红色又变成紫色,
H2CO3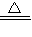 H2O+CO2↑;
H2O+CO2↑;
(5)硝酸银在日照条件下生成银、二氧化氮和氧气,2AgNO3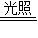 2Ag+2NO2↑+O2↑,+根据化合物中正负化合价的代数和为0,可分别求出AgNO3、NO2中氮元素的化合价为+5、+4价;
2Ag+2NO2↑+O2↑,+根据化合物中正负化合价的代数和为0,可分别求出AgNO3、NO2中氮元素的化合价为+5、+4价;
故答案为:
(1)Ca(OH)2+CO2═CaCO3↓+H2O
(2)3CO+Fe2O3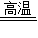 2Fe+3CO2
2Fe+3CO2
(3)4Al+3MnO2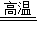 3Mn+2Al2O3
3Mn+2Al2O3
(4)紫色变红色,红色变紫色,H2CO3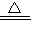 H2O+CO2↑,紫色逐渐变浅,活性炭具有吸附性
H2O+CO2↑,紫色逐渐变浅,活性炭具有吸附性
(5))2AgNO3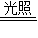 2Ag+2NO2↑+O2↑,+5、+4.
2Ag+2NO2↑+O2↑,+5、+4.
点评:本题主要考查化学方程式的书写,难度稍大.
解答:解:(1)二氧化碳与氢氧化钙反应生成碳酸钙和水,Ca(OH)2+CO2═CaCO3↓+H2O;
(2)一氧化碳与氧化铁反应生成铁和二氧化碳,3CO+Fe2O3
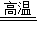 2Fe+3CO2;
2Fe+3CO2;(3)铝和二氧化锰在高温条件下生成锰和氧化铝4Al+3MnO2
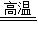 3Mn+2Al2O3;
3Mn+2Al2O3;(4)二氧化碳与水反应生成碳酸,碳酸使紫色石蕊变红,加热后碳酸分解生成水和二氧化碳,红色又变成紫色,
H2CO3
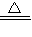 H2O+CO2↑;
H2O+CO2↑;(5)硝酸银在日照条件下生成银、二氧化氮和氧气,2AgNO3
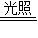 2Ag+2NO2↑+O2↑,+根据化合物中正负化合价的代数和为0,可分别求出AgNO3、NO2中氮元素的化合价为+5、+4价;
2Ag+2NO2↑+O2↑,+根据化合物中正负化合价的代数和为0,可分别求出AgNO3、NO2中氮元素的化合价为+5、+4价;故答案为:
(1)Ca(OH)2+CO2═CaCO3↓+H2O
(2)3CO+Fe2O3
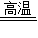 2Fe+3CO2
2Fe+3CO2(3)4Al+3MnO2
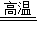 3Mn+2Al2O3
3Mn+2Al2O3(4)紫色变红色,红色变紫色,H2CO3
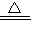 H2O+CO2↑,紫色逐渐变浅,活性炭具有吸附性
H2O+CO2↑,紫色逐渐变浅,活性炭具有吸附性(5))2AgNO3
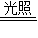 2Ag+2NO2↑+O2↑,+5、+4.
2Ag+2NO2↑+O2↑,+5、+4.点评:本题主要考查化学方程式的书写,难度稍大.

练习册系列答案
相关题目
汽车作为一种常见交通工具,已走进千家万户。请回答下列问题:
(1) 目前汽车使用的燃料是汽油。将石油加热,利用各成分的沸点不同将它们分离可得到汽油,该过程属于 变化。
![]() 我国已推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇,作为汽车的燃料。下列叙述正确的是 。(填字母)
我国已推广使用车用乙醇汽油,它是在汽油中加入适量的乙醇,作为汽车的燃料。下列叙述正确的是 。(填字母)
A.乙醇汽油是一种新型的化合物 B.乙醇可通过粮食发酵的方法制得
C.使用乙醇汽油能减少有害气体的排放 D.乙醇和汽油都是可再生能源
(2)汽车尾气(含有CO、NO等物质)是城市空气的污染物,治理的方法之一是在汽车的排气管上装一个催化转换器,使CO和NO反应,生成两种无毒气体,试写出CO与NO反应的化学方程式 。
(3)汽车生产过程中需要各种金属,其中用量最大的是铁和铝。
①工业上炼铁的简要流程如下:
 |
请写出步骤Ⅰ、Ⅱ、Ⅲ的化学反应方式 、 、 。
② 早在西汉时期,我国劳动人民就利用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”,即反应③,若用该方法制得铜16千克,理论上需要溶质质量分数为10%的硫酸铜溶液多少千克?(写计算过程)
氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
(1)你认为用这种方法制氧气的优点是;
(2)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①简述检查装置气密性的方法;
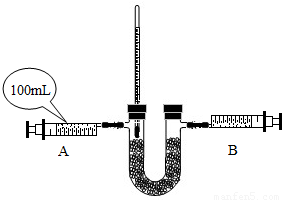
②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量;
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,
说明反应(填“吸热”或“放热”),同时还可以观察到固体粉末发生变化的现象是;
(3)小红同学通过查阅资料了解到Na2O2还能与水反应,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.于是她根据这一原理设计了一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形瓶中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上,观察显示数字的变化,并记录(数据见下表);③进行计算.
a.从上表数据判断,秒时已经反应完全;
b.请你帮小红同学计算此样品中Na2O2的纯度为(不需要写出计算过程).
(4)Na2O2露置在空气中容易发生变质,如何检验已经变质,简述实验方法、现象和结论..
(1)你认为用这种方法制氧气的优点是;
(2)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①简述检查装置气密性的方法;
②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量;
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,
说明反应(填“吸热”或“放热”),同时还可以观察到固体粉末发生变化的现象是;
(3)小红同学通过查阅资料了解到Na2O2还能与水反应,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑.于是她根据这一原理设计了一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形瓶中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上,观察显示数字的变化,并记录(数据见下表);③进行计算.
| 时间/s | 60 | 120 | 180 | 240 | 300 | |
| 天平示数/g | 85.00 | 83.82 | 82.43 | 82.15 | 81.80 | 81.80 |
b.请你帮小红同学计算此样品中Na2O2的纯度为(不需要写出计算过程).
(4)Na2O2露置在空气中容易发生变质,如何检验已经变质,简述实验方法、现象和结论..

 37、氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
37、氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2.
 汽车作为一种常见交通工具,已走进千家万户.请回答下列问题:
汽车作为一种常见交通工具,已走进千家万户.请回答下列问题:
 汽车作为一种常见交通工具,已走进千家万户.请回答下列问题:
汽车作为一种常见交通工具,已走进千家万户.请回答下列问题: