题目内容
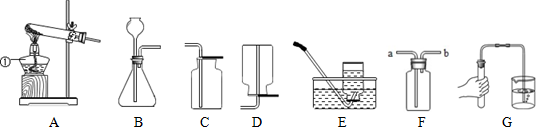
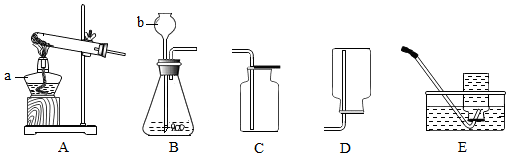
5.小强和几位同学在实验室用下列装置制取几种气体.
(1)写出图中标有的仪器名称:①试管②酒精灯;
(2)小强想用高锰酸钾制取较纯净的氧气,他应选择上述装置中的A和D(填字母)进行组装,写出该反应的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,加热时试管口要略向下倾斜的原因是防止冷凝水倒流而使试管破裂.
(3)小翔选用B和C装置制取氧气,写出反应的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.验满氧气的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
分析 试管是常用的反应容器,酒精灯是常用的加热仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净.氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
解答 解:(1)试管是常用的反应容器,酒精灯是常用的加热仪器,故答案为:试管;酒精灯;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;加热时试管口要略向下倾斜的原因是:防止冷凝水倒流而使试管破裂;故答案为:D;高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;防止冷凝水倒流而使试管破裂;
(3)如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;氧气的验满方法是:将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;故答案为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气;将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
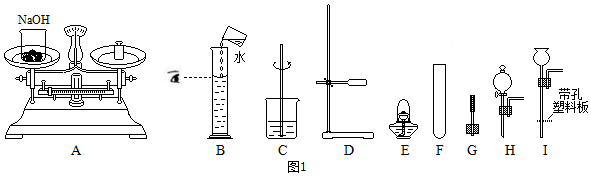
6.下列图示实验基本操作正确的是( )
| A. | 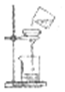 | B. |  | C. |  | D. | 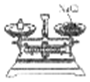 |
7.如图所示的实验操作中正确的是( )
| A. |  | B. |  | C. |  | D. |  |
17.某校化学兴趣小组的同学对一瓶存放已久的氢氧化钠溶液产生浓厚的兴趣,他们探究该溶液是否变质的过程如下:
【提出问题】该氢氧化钠溶液是否变质?
【猜想与假设】
猜想①:氢氧化钠溶液可能全部变质,其溶质是Na2CO3(填化学式,下同)
猜想②:氢氧化钠溶液可能部分变质,其溶质是NaOH、Na2CO3.
猜想③:氢氧化钠溶液没有变质,其溶质是NaOH
【实验探究】
【实验结论】综合上述实验(1)、(2),你得出的结论是猜想②成立.
【反思拓展】(1)氢氧化钠露置于空气中容易变质,原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是反应物是否过量.
【提出问题】该氢氧化钠溶液是否变质?
【猜想与假设】
猜想①:氢氧化钠溶液可能全部变质,其溶质是Na2CO3(填化学式,下同)
猜想②:氢氧化钠溶液可能部分变质,其溶质是NaOH、Na2CO3.
猜想③:氢氧化钠溶液没有变质,其溶质是NaOH
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加足量的氯化钡溶液 | 产生白色沉淀 | 原溶液中一定有碳酸钠 |
| (2)取(1)反应后的上层清液于试管中,滴加无色酚酞试液 | 溶液成红色 | 原溶液中一定有氢氧化钠 |
【反思拓展】(1)氢氧化钠露置于空气中容易变质,原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示).
(2)在分析化学反应的物质成分时,除了考虑生成物外,还需考虑的是反应物是否过量.
14.下列物质能溶于水的是( )
| A. | AgCl | B. | BaSO4 | C. | Ca(NO3)2 | D. | Fe(OH)3 |
15.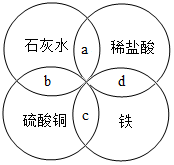 铁、盐酸、石灰水、硫酸铜是科学实验室中常见的物质,四种物质间的 反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的主要实验现象,其中描述正确的是( )
铁、盐酸、石灰水、硫酸铜是科学实验室中常见的物质,四种物质间的 反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的主要实验现象,其中描述正确的是( )
 铁、盐酸、石灰水、硫酸铜是科学实验室中常见的物质,四种物质间的 反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的主要实验现象,其中描述正确的是( )
铁、盐酸、石灰水、硫酸铜是科学实验室中常见的物质,四种物质间的 反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的主要实验现象,其中描述正确的是( )| A. | a有气泡产生 | B. | b无明显现象 | C. | c有红色固体析出 | D. | d有蓝色沉淀生成 |