题目内容
19.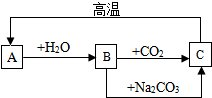 (1)A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物已略去),请按要求回答有关问题:
(1)A、B、C是三种常见的含钙化合物,它们之间有如图所示的转化关系(部分产物已略去),请按要求回答有关问题:①A物质的化学式是CaO.
②B的澄清溶液可用来检验二氧化碳气体,其实验现象是澄清石灰水变浑浊.
③写出B物质与Na2CO3反应的化学方程式Ca(OH)2+Na2CO3═2NaOH+CaCO3↓,该反应属于基本反应类型中的复分解反应.
(2)在Cu(NO3)2、Ag NO3、Al(NO3)3混合溶液中,加入一定量的Fe粉,充分反应后过滤,则滤液中一定含有的金属离子是Al3+、Fe2+(填离子符号).
分析 (1)根据A、B、C是三种常见的含钙化合物,A和水反应会生成B,B和二氧化碳会生成C,C在高温的条件下会生成A,所以A是氧化钙,氧化钙和水会生成氢氧化钙,所以B是氢氧化钙,氢氧化钙和二氧化碳会生成碳酸钙沉淀和水,所以C是碳酸钙,然后将推出的各种物质代入转化关系中验证即可.
(2)根据金属银、铜、铁的活动性由强到弱的顺序铝>铁>铜>银,当把铁粉加入到AgNO3、Cu(NO3)2、Al(NO3)3的混合溶液中,首先置换出银,银被置换完后才继续置换铜,但不能置换铝等知识进行分析.
解答 解:(1)①A、B、C是三种常见的含钙化合物,A和水反应会生成B,B和二氧化碳会生成C,C在高温的条件下会生成A,所以A是氧化钙,氧化钙和水会生成氢氧化钙,所以B是氢氧化钙,氢氧化钙和二氧化碳会生成碳酸钙沉淀和水,所以C是碳酸钙,氧化钙和水生成氢氧化钙,氢氧化钙和二氧化碳会生成碳酸钙沉淀,氢氧化钙和碳酸钠会生成碳酸钙沉淀和氢氧化钠,碳酸钙高温会生成氧化钙和二氧化碳,推出的各种物质均满足题意,推导合理,所以A物质的化学式是:CaO;
②通过推导可知B是氢氧化钙溶液,氢氧化钙溶液和二氧化碳反应会生成碳酸钙沉淀和水,所以B的澄清溶液可用来检验二氧化碳气体,其实验现象是:澄清石灰水变浑浊,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
③B物质与Na2CO3的反应是氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3=2NaOH+CaCO3↓;
(2)金属银、铜、铁的活动性由强到弱的顺序铝>铁>铜>银,当把铁粉加入到AgNO3、Cu(NO3)2、Al(NO3)3的混合溶液中,首先置换出银,银被置换完后才继续置换铜,但不能置换铝,所以溶液中一定有硝酸铝和硝酸亚铁.
故答案为:(1)①CaO ②澄清石灰水变浑浊
③Ca(OH)2+Na2CO3═2NaOH+CaCO3↓ 复分解反应
(2)Al3+、Fe2+
点评 在解推断题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案| A. | 小苏打用于焙制糕点 | B. | 浓硫酸做干燥剂 | ||
| C. | 二氧化碳做温室肥料 | D. | 盐酸用于除锈 |
| A. | 冰雪融化 | B. | 红磷燃烧 | C. | 食物腐烂 | D. | 葡萄酿酒 |
| A. |  向盐酸和氯化铁的混合溶液中滴加过量的氢氧化钠溶液 | |
| B. |  某温度下,向一定量接近饱和的硝酸钾溶液中加入足量硝酸钾固体 | |
| C. |  加热一定量的高锰酸钾制氧气 | |
| D. |  氯酸钾和二氧化锰混合加热制取氧气 |
【提出问题】为什么会有气体产生?
【查阅资料】硫酸铜溶液呈酸性.
【讨论】(1)pH小于7的溶液不一定(填“一定”或“不一定”)是酸溶液;
(2)某同学用湿润的pH试纸测定该溶液的酸碱度,其测定的结果是偏大(填“偏大”、“偏小”或“无影响”);
【继续探究】该气体成分是什么?
【提出猜想】①可能是二氧化碳;②可能是氢气;③可能是二氧化硫.你认为还可能的是氧气;
【设计实验】(1)小欣发现此气体没有气味,则猜想③是错误的;他认为猜想①也不对,理由是反应物中没有碳元素,不会生成二氧化碳气体;
(2)小欣对剩余的两种猜想进行了如下实验:
| 实验步骤 | 现象 | 结论 |
| 取一试管气体 点燃 | 发现轻微的爆鸣声,并产生淡蓝色火焰 | 猜想②正确 |
| A. | 生理盐水 | B. | 止咳糖浆 | C. | 液氧 | D. | 碘酒 |
 我国具有丰富的煤炭资源,煤制取乙二醇的产业化发展已列入我国石化石化产业调整和振兴规划,由煤制取乙二醇的流程示意图为:
我国具有丰富的煤炭资源,煤制取乙二醇的产业化发展已列入我国石化石化产业调整和振兴规划,由煤制取乙二醇的流程示意图为: