题目内容
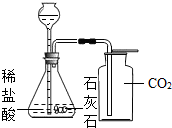
为测定石灰石中碳酸钙的质量分数,化学兴趣小组的同学设计了以下方案:将94.9 g稀盐酸加入到15 g石灰石样品中,恰好完全反应.生成的二氧化碳气体全部用足量的NaOH溶液吸收,NaOH溶液增加的质量随时问变化如下表:(友情提示:石灰石中的杂质不参加反应且难溶于水)
求:(1)最终生成CO2的质量________;
(2)样品中CaCO3的质量分数(计算结果精确到0.1%);
(3)将石灰石与稀盐酸反应后的剩余物质进行过滤,再向滤液中加入多少克水可以得到10%的CaCl2溶液.
答案:
解析:
解析:
|
(l)4.4 g(1分) 答;(2)CaCO3的质量分数为66.7% (3)所需加永的质量为11 g. 解:(2)设样品中CaCO3的质量为x.生成CaCl2的质量为y,加入水的质量为z.(1分) x=10 g(1分) CaCO3的质量分数= (3) y=11.1 g(1分) z=11 g(1分) 补充说明:试卷中要求只答一种或一条的,多答的内容无效. |

练习册系列答案
相关题目
为测定石灰石中碳酸钙的质量分数,化学兴趣小组的同学设计了以下方案:将94.4g稀盐酸加入到15g石灰石样品中,恰好完全反应.生成的二氧化碳气体全部用足量的NaOH溶液吸收,NaOH溶液增加的质量随时问变化如下表:(友情提示:石灰石中的杂质不参加反应且难溶于水)
求:(1)最终生成CO2的质量 ;
(2)样品中CaCO3的质量分数(计算结果精确到0.1%);
(3)将石灰石与稀盐酸反应后的剩余物质进行过滤,再向滤液中加入多少克水可以得到10%的CaCl2溶液.
| 时间(min) | t1 | t2 | t3 | t4 | t | t6 | t7 | t8 |
| 氢氧化钠溶液增加的质量(g) | 1.5 | 2 | 2.5 | 3 | 3.5 | 4 | 4.4 | 4.4 |
(2)样品中CaCO3的质量分数(计算结果精确到0.1%);
(3)将石灰石与稀盐酸反应后的剩余物质进行过滤,再向滤液中加入多少克水可以得到10%的CaCl2溶液.
我县西田各庄镇西智地区山上含有大量石灰石(主要成分为碳酸钙),为测定石灰石中碳酸钙的含量,某学校课外小组同学做了如下实验:首先称取50g该地区的石灰石样品,然后将150mL的稀盐酸分5次加入(假设其余杂质均不与盐酸反应)进行充分反应.实验过程中的数据记录如下
(1)X= g;
(2)计算该石灰石样品中碳酸钙的质量分数是多少?
(3)若把该反应产生的二氧化碳全部收集起来,共有多少L?
(注意:①二氧化碳气体的密度为1.977g/L,②要求写出全部计算过程)
| 稀盐酸的体积 | 第一次30mL | 第二次30mL | 第三次30mL | 第四次30mL | 第五次30mL |
| 剩余固体质量 | 40.0g | X | 20.0g | 10.0g | 5.0g |
(2)计算该石灰石样品中碳酸钙的质量分数是多少?
(3)若把该反应产生的二氧化碳全部收集起来,共有多少L?
(注意:①二氧化碳气体的密度为1.977g/L,②要求写出全部计算过程)